题目内容
【题目】某次硫酸铜晶体结晶水含量的测定实验中,相对误差为+2.7%,其原因不可能是( )
A.实验时坩埚未完全干燥B.加热后固体未放入干燥器中冷却
C.加热过程中晶体有少量溅失D.加热后固体颜色有少量变黑
【答案】B
【解析】
A.实验时坩埚未完全干燥,计算出的结晶水的质量偏高,会使误差偏大,故A错误;
B.加热后固体未放入干燥器中冷却,固体部分吸水,差距值变小,结果偏小,故B正确;
C.加热过程中晶体有少量溅失,固体质量减少得多,结晶水含量测得值会偏高,故C错误;
D.加热后固体颜色有少量变黑,说明部分硫酸铜分解,导致计算出的结晶水的质量偏高,测定结果偏高,故D错误;
故答案为B。

练习册系列答案
相关题目
【题目】如下图所示的实验装置用于研究温度对凝乳酶催化乳汁凝固的影响。
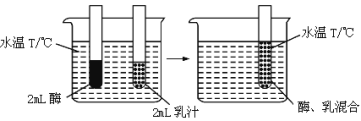
先将酶和乳汁分别装入2支试管中,再将2支试管放入同一水浴(温度用℃表示)环境中持续15min,最后将酶和乳汁倒入同一试管中混合,保温并记录凝乳所需要的时间。多次实验并记录在不同温度下所需要的时间,其结果记于下表:
装置 | A | B | C | D | E | F |
水浴温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 |
凝乳时间(min) | 很长 | 7.0 | 4.0 | 1.5 | 4.0 | 不凝乳 |
(1)解释以下两种处理对实验结果的影响。
①将装置A中的混合物加温至40℃,乳汁凝固时间如何变化? (明显缩短/明显增加/时间不变/不会凝固)
②装置F中的混合物冷却至40℃, 乳汁凝固时间如何变化? (明显缩短/明显增加/时间不变/不会凝固)。原因是 。
(2)若将酶和乳汁先混合再进行F组实验,实验结果会不准确,原因是什么 。
(3)为进一步探究该酶催化作用的最适温度,应在 范围内设置更小的温度梯度,其他条件不变,重新进行实验,凝乳时间最短对应的温度接近最适温度。