题目内容
1.X、Y、Z、W为电子数相同的分子或离子.X有5个原子核.通常状况下,W为无色液体.它们之间转化关系如图1所示: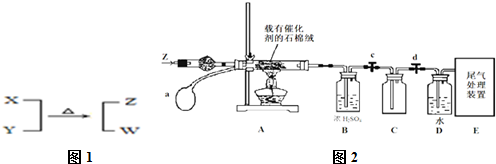
请回答:
(1)Z的电子式是
 .
.(2)实验室制取Z的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2.
(3)某化学小组同学模拟工业生产制取HNO3,设计如图2所示装置,其中a为一个可持续鼓入空气的橡皮球.
①A中发生反应的化学方程式是4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
②B中浓H2SO4的作用是吸收水与未反应的氨气.
(4)写出D装置中反应的化学方程式3NO2+H2O=2HNO3+NO.
分析 X、Y、Z、W为电子数相同的分子或离子,X有5个原子核.通常状况下,W为无色液体,发生反应X+Y$\stackrel{△}{→}$Z+W,应是NH4++OH-=NH3↑+H2O,推断X为NH4+、Y为OH-、Z为NH3、W为H2O.
(1)Z为NH3,分子中N原子与H原子之间形成1对共用电子对,N原子含有1对孤电子对;
(2)实验室用氢氧化钙与氯化铵再加热条件下制备氨气,反应生成氯化钙、氨气与水;
(3)①A中发生氨的催化氧化,氨气与氧气反应生成NO与水;
②吸收水与未反应的氨气;
(4)D中为二氧化氮与水反应生成硝酸与NO.
解答 解:X、Y、Z、W为电子数相同的分子或离子,X有5个原子核.通常状况下,W为无色液体,发生反应X+Y$\stackrel{△}{→}$Z+W,应是NH4++OH-=NH3↑+H2O,推断X为NH4+、Y为OH-、Z为NH3、W为H2O.
(1)Z为NH3,分子中N原子与H原子之间形成1对共用电子对,N原子含有1对孤电子对,电子式为 ,故答案为:
,故答案为: ;
;
(2)实验室用氢氧化钙与氯化铵再加热条件下制备氨气,反应生成氯化钙、氨气与水,反应方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2;
(3)①A中发生氨的催化氧化,氨气与氧气反应生成NO与水,反应方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
②浓硫酸作用是吸收水与未反应的氨气,故答案为:吸收水与未反应的氨气;
(4)D中为二氧化氮与水反应生成硝酸与NO,反应方程式为3NO2+H2O=2HNO3+NO,故答案为:3NO2+H2O=2HNO3+NO.
点评 本题考查无机物推断、硝酸的制备等,题目比较综合,推断物质是解题关键,注意识记常见10电子、18电子微粒,难度中等.

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案| A. | 要完成实验需称取10.6gNa2CO3﹒10H2O晶体 | |
| B. | 本实验需用到的仪器是天平、药匙、玻璃棒、烧杯、100mL容量瓶 | |
| C. | 配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低 | |
| D. | 定容时俯视刻度线会导致浓度偏高 |
| A. | 消去 | B. | 加成 | C. | 取代 | D. | 氧化 |
| A. | 将FeCl3饱和溶液滴入沸水中可制得Fe(OH)3胶体 | |
| B. | AlCl3溶液和Al2(SO4)3溶液加热蒸干、灼烧都得到Al2O3 | |
| C. | 向FeBr2溶液中通入过量Cl2,加CCl4振荡静置,上层液体无色、下层为橙红色 | |
| D. | 将Cl2通入Na2SO3溶液中,检验是否有SO42-生成,可向该溶液中滴加足量盐酸酸化的Ba(NO3)2溶液 |
| A. | NaOH | B. | CH4 | C. | HCl | D. | H2O2 |
| A. | 向待测溶液中加入AgNO3溶液出现白色沉淀,原溶液中一定含有Cl- | |
| B. | 用AgNO3溶液检验Cl-、Br-、I-时,必须用稀盐酸进行酸化 | |
| C. | 可以用新制的氨水和CCl4来鉴别Cl-、Br-、I- | |
| D. | 向某白色沉淀中加入稀硝酸,产生使澄清石灰水变浑浊的气体,则原白色沉淀一定为Ag2CO3 |
