题目内容
16.丙烯酸结构如下,下列说法不正确的是( )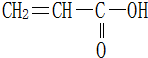
| A. | 它可以使溴的四氯化碳溶液褪色 | B. | 它可以使酸性高锰酸钾溶液褪色 | ||
| C. | 它与醋酸属于同系物 | D. | 它可与金属钠反应 |
分析 CH2=CH-COOH含有C=C和-COOH,C=C可发生加成、加聚以及氧化反应,-COOH具有酸性,可发生酯化反应.
解答 解:A.含有碳碳双键,可与溴发生加成反应,故A正确;
B.含有碳碳双键,可被酸性高锰酸钾氧化,故B正确;
C.含有碳碳双键,与醋酸结构不同,不是同系物,故C错误;
D.含有羧基,与金属钠反应生成氢气,故D正确.
故选C.
点评 本题考查有机物的结构和性质,题目难度不大,注意把握有机物的官能团的结构和性质,为解答该类题目的关键.

练习册系列答案
相关题目
3.设阿伏加德罗常数为NA,下列说法不正确的是( )
| A. | 71g Cl2所含的原子数为2NA | |
| B. | 18g水中所含电子数为10 NA | |
| C. | 24g Mg与足量的盐酸反应转移电子数为 NA | |
| D. | 在1L 2mol/L的硝酸镁溶液中含有的硝酸根离子数为4 NA |
11.用含有A1203、SiO2和少量FeO•xFe2O3的铝灰制备A12(SO4)3•18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品.
(1)H2S04溶解A1203的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)MnO4- 氧化Fe2+的离子方程式补充完整:1MnO4-+5Fe2++8H+=1Mn2++5Fe3++4H2O
(3)已知:生成氢氧话务沉淀的pH
注:金属离子的起始浓度为0.1mol.L-1
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀
(4)己知:一定条件下,MnO4- 可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnS04的目的是除去过量的MnO4-.
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品.
(1)H2S04溶解A1203的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)MnO4- 氧化Fe2+的离子方程式补充完整:1MnO4-+5Fe2++8H+=1Mn2++5Fe3++4H2O
(3)已知:生成氢氧话务沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀
(4)己知:一定条件下,MnO4- 可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnS04的目的是除去过量的MnO4-.
1.下列对“可能”说法不正确的是( )
| A. | 原子晶体中可能存在非极性共价键 | |
| B. | 金属晶体可能比分子晶体熔点低 | |
| C. | 干冰升华时,分子内共价键可能会发生断裂 | |
| D. | 金属元素和非金属元素形成的化合物可能是离子化合物 |
6.下列各组中两个变化所发生的反应,属于同一类型的是( )
| A. | 由甲苯制甲基环己烷、由乙烷制溴乙烷 | |
| B. | 乙烯使溴水褪色、乙炔使酸性高锰酸钾水溶液褪色 | |
| C. | 由乙烯制聚乙烯、由氯乙烯制聚氯乙烯 | |
| D. | 由苯制硝基苯、由溴乙烷制取乙醇 |