题目内容
3.设阿伏加德罗常数为NA,下列说法不正确的是( )| A. | 71g Cl2所含的原子数为2NA | |
| B. | 18g水中所含电子数为10 NA | |
| C. | 24g Mg与足量的盐酸反应转移电子数为 NA | |
| D. | 在1L 2mol/L的硝酸镁溶液中含有的硝酸根离子数为4 NA |
分析 A、求出氯气的物质的量n=$\frac{m}{M}$,然后根据1mol氯气中含2mol氯原子来分析;
B、求出水的物质的量n=$\frac{m}{M}$,然后根据1mol水中含10mol电子来分析;
C、求出镁的物质的量n=$\frac{m}{M}$,然后根据反应后镁变为+2价来分析;
D、求出硝酸镁的物质的量n=CV,然后根据1mol硝酸镁中含2mol硝酸根来分析.
解答 解:A、71g氯气的物质的量n=$\frac{m}{M}$=$\frac{71g}{71g/mol}$=1mol,而1mol氯气中含2mol氯原子即2NA个,故A正确;
B、18g水的物质的量n=$\frac{m}{M}$=$\frac{18g}{18g/mol}$=1mol,而1mol水中含10mol电子即10NA个,故B正确;
C、24g镁的物质的量n=$\frac{m}{M}$=$\frac{24g}{24g/mol}$=1mol,而反应后镁变为+2价,故1mol镁转移2mol电子即2NA个,故C错误;
D、硝酸镁的物质的量n=CV=2mol/L×1L=2mol,1mol硝酸镁中含2mol硝酸根,故2mol硝酸镁中含4mol硝酸根即4NA个,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
13.已知某温度时,反应X2(g)+Y2(g)?2XY(g)的平衡常数K=20,由此推测在该温度时,反应2XY(g)?X2(g)+Y2(g)的化学平衡常数为( )
| A. | 20 | B. | 50 | C. | 0.05 | D. | 无法确定 |
11.下列实验能成功的( )
| A. | 乙醇和浓硫酸加热到140℃制取乙烯 | |
| B. | 乙烷和氯气光照下制取纯净的氯乙烷 | |
| C. | 在苯和溴水的混合物中加入铁粉制取溴苯 | |
| D. | 用酸性高锰酸钾溶液区分 和 和 |
18.下列各组指定的元素,不能形成AB2型化合物的是( )
| A. | 2s22p2和2s22p4 | B. | 3s1和3s23p5 | C. | 3s2和3s23p5 | D. | 3s23p4和2s22p2 |
8.铀主要有两种同位素,关于${\;}_{92}^{235}U$的说法正确的是( )
| A. | 质子数为92 | B. | 中子数为235 | C. | 核外电子数为143 | D. | 质量数为92 |
15.Fe(OH)3胶体和MgCl2溶液共同具有的性质是( )
| A. | 都不稳定,密闭放置可产生沉淀 | |
| B. | 两者都有“丁达尔效应” | |
| C. | 加入氢氧化钠溶液二者都能沉淀,Fe(OH)3胶体发生聚沉,MgCl2发生化学反应生成沉淀 | |
| D. | 两者都能透过半透膜 |
12.下面关于电解质的叙述中正确的是( )
| A. | 化合物电离时,生成的阳离子是氢离子的是酸 | |
| B. | 电解质、非电解质都指化合物而言,单质不属于此范畴 | |
| C. | 电解质在水中一定能导电 | |
| D. | 纯水的导电性很差,所以水不是电解质 |
16.丙烯酸结构如下,下列说法不正确的是( )
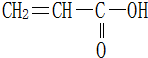
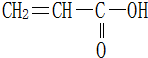
| A. | 它可以使溴的四氯化碳溶液褪色 | B. | 它可以使酸性高锰酸钾溶液褪色 | ||
| C. | 它与醋酸属于同系物 | D. | 它可与金属钠反应 |
 .
.