题目内容
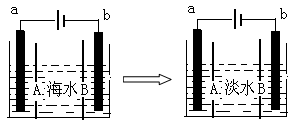
电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO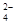 等离子,电极为惰性电极。下列叙述中正确的是
等离子,电极为惰性电极。下列叙述中正确的是
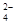 等离子,电极为惰性电极。下列叙述中正确的是
等离子,电极为惰性电极。下列叙述中正确的是
| A.A膜是阳离子交换膜 |
| B.通电后,海水中阴离子往b电极处运动 |
| C.通电后,b电极上产生无色气体,溶液中出现白色沉淀 |
| D.通电后,a电极的电极反应式为:4OH--4e- = O2↑+2H2O |
C
试题分析:A.A膜是阴离子交换膜。错误。B.通电后,海水中阴离子往正电荷较多的阳极a电极处运动.错误。C.通电后,由于放电能力H+>Mg2+>Ca2+,所以H+在阴极b电极上放电:2H++2e-=H2↑.产生无色气体,由于破坏了附近的水的电离平衡,在该区域c(OH-)增大,会发生反应:Mg2++2OH-=Mg(OH)2↓所以溶液中还出现白色沉淀。正确。D.通电后,由于在溶液中的放电能力Cl->SO
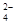 .所以在阳极发生反应:2Cl-—2e-=Cl2↑。错误。
.所以在阳极发生反应:2Cl-—2e-=Cl2↑。错误。
练习册系列答案
相关题目

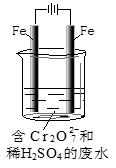
 KIO3 + 3H2↑。下列有关说法正确的是
KIO3 + 3H2↑。下列有关说法正确的是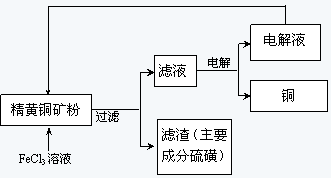

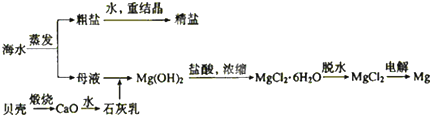
 ,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是
,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是