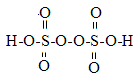��Ŀ����
KClO3��ŨHCl��һ���¶��·�Ӧ�����ɻ���ɫ���ױ���������ȡ��䷴Ӧ�ɱ���Ϊ��
KClO3+ HCl(Ũ)�� KCl+ ClO2+ Cl2+ H2O
��1����ƽ���ϻ�ѧ����ʽ(��ѧ���������뻮����)����˫���ű������ת�Ƶķ������Ŀ��
��2����Ӧ�е��������� �� ClO2�Ƿ�Ӧ�� (��������ԭ)���
��3����Ӧ����0.1 mol Cl2����ת�Ƶĵ��ӵ����ʵ���Ϊ mol��
��4��ClO2���к�ǿ�������ԣ���˿ɱ�����������������ClO2����������������ת��ΪCl-������������Ч��(�Ե�λ���ʵ����õ���������ʾ)��Cl2�� ����
KClO3+ HCl(Ũ)�� KCl+ ClO2+ Cl2+ H2O
��1����ƽ���ϻ�ѧ����ʽ(��ѧ���������뻮����)����˫���ű������ת�Ƶķ������Ŀ��
��2����Ӧ�е��������� �� ClO2�Ƿ�Ӧ�� (��������ԭ)���
��3����Ӧ����0.1 mol Cl2����ת�Ƶĵ��ӵ����ʵ���Ϊ mol��
��4��ClO2���к�ǿ�������ԣ���˿ɱ�����������������ClO2����������������ת��ΪCl-������������Ч��(�Ե�λ���ʵ����õ���������ʾ)��Cl2�� ����
��1�� ��2�֣�
��2�֣�
��2��KClO3 ��1�֣� ��ԭ ��1�֣� ��3��0.2mol ��1�֣� ��4��2.5�� (1��)
 ��2�֣�
��2�֣���2��KClO3 ��1�֣� ��ԭ ��1�֣� ��3��0.2mol ��1�֣� ��4��2.5�� (1��)
�����������1��KClO3����Ԫ�ػ��ϼ���+5�۽���ΪClO2��+4�ۣ��õ�1�����ӣ����������������HCl����Ԫ�ػ��ϼ���-1������ΪCl2��0�ۣ�ʧȥ1�����ӣ��Ȼ����ǻ�ԭ�������ݵ��ӵ�ʧ�غ��֪���������뻹ԭ�������ʵ���֮����1:1�����KClO3ϵ��Ϊ2��ClO2ϵ��Ϊ2��KClϵ��Ϊ2��Cl2ϵ��Ϊ1����HClϵ��Ϊ4�����ԭ���غ��֪ˮ��ϵ����2����˸÷�Ӧ����ת�Ƶķ������Ŀ�ɱ�ʾΪ
 ��
����2����Ӧ2KClO3+4HCl��Ũ����2KCl+Cl2��+2ClO2��+2H2O�У���KClO3����Ԫ�ػ��ϼ��ɣ�1�۽���ΪClO2�У�4�ۿ�֪��KClO3����Ԫ�ر���ԭ������KClO3����������ClO2�ǻ�ԭ���
��3����Ӧ��ֻ��Cl2���������HCl����Ԫ�ػ��ϼ���-1������ΪCl2��0�ۣ����Բ���0.1molCl2ת�Ƶĵ��ӵ����ʵ���Ϊ0.1mol��2��0.2mol��
��4��1molCl2���Ի��2mol���ӣ�ClO2����������������ת��ΪCl-����˵��1molClO2���Ի��5mol���ӣ�����ClO2������Ч����Cl2��
 ��2.5����
��2.5����
��ϰ��ϵ�д�
�����Ŀ
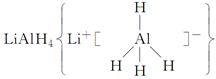 ��LiH���ǽ���������������л��ϳ��еij����Լ�����ˮ���ܾ��ҷ�Ӧ�ų�H2��LiAlH4��125 ��ֽ�ΪLiH��H2��Al������˵���в���ȷ���� (����)��
��LiH���ǽ���������������л��ϳ��еij����Լ�����ˮ���ܾ��ҷ�Ӧ�ų�H2��LiAlH4��125 ��ֽ�ΪLiH��H2��Al������˵���в���ȷ���� (����)��