题目内容
9.将如下卤化物跟浓硫酸放在烧瓶中共热可以得到纯净卤化氢气体的是( )| A. | NaF | B. | NaCl | C. | NaBr | D. | NaI |
分析 浓硫酸具有强氧化性、难挥发性,能氧化某些强还原性的氢化物,氢氟酸能够与玻璃中的二氧化硅反应生成四氟化硅,据此解答.
解答 解:A.氟化钠与浓硫酸反应生成氢氟酸,氢氟酸与玻璃中的二氧化硅反应生成四氟化硅,所以得到气体不纯净,故A不选;
B.浓硫酸难挥发,氯化氢易挥发,能够与氯化钠反应制备氯化氢,故B选;
C.溴化氢具有强的还原性,能够被浓硫酸氧化,得到气体不纯净,故C不选;
D.碘化氢具有强的还原性,能够别浓硫酸氧化,得到的气体不纯净,故D不选;
故选:B.
点评 本题考查了氢化物的制取,明确浓硫酸难挥发性、强的氧化性的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
19.下列关于铝单质的叙述中正确的是( )
| A. | 由于铝在空气中不会锈蚀,所以铝制品的使用寿命都很长 | |
| B. | 由于铝具有强还原性,所以常用铝来冶炼某些高熔点金属 | |
| C. | 常温下,铝遇浓硫酸钝化,所以可用浓硫酸除去铝表面的铜镀层 | |
| D. | 由于铝的导电性比铜强,所以常用铝制造电线、电缆 |
20.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,4.48L水中含有的分子数为0.2NA | |
| B. | 1L 1mol•L-1 CaCl2溶液中含有的氯离子数为NA | |
| C. | 25℃,1.01×105Pa时,32gO2和O3的混合气体中含有的原子数为25NA | |
| D. | 在常温常压下,44gCO2中含有的原子数为3NA |
14.下列说法不正确的是( )
| A. | 化学实验中多余剩下的钠固体要放回原试剂瓶 | |
| B. | 分液漏斗和容量瓶实验使用前都要检验是否漏水 | |
| C. | 加热煮沸FeCl3饱和溶液至红褐色,所得液体有丁达尔效应 | |
| D. | 纯净的SiO2晶体可用于制作光导纤维的材料 |
1.下列反应中,属于吸热反应的是( )
| A. | 氢氧化钡晶体与氯化铵晶体反应 | B. | 氢气在氯气中燃烧 | ||
| C. | 氢氧化钠溶液与盐酸反应 | D. | 钠与水反应 |
18.下列说法中正确的是( )
| A. | CH3Cl,CH2Cl2,CHCl3水解的最终产物都是CH3OH | |
| B. | 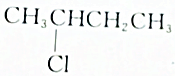 发生消去反应的产物不只一种 发生消去反应的产物不只一种 | |
| C. | 将溴苯加入到AgNO3溶液中,立即有淡黄色沉淀生成 | |
| D. | 1,2-二溴乙烷在NaOH的水溶液中共热可得到乙炔 |
19.下列电离方程式中正确的是( )
| A. | Na2CO3$\frac{\underline{\;通电\;}}{\;}$2Na++CO32- | B. | MgSO4═Mg2++SO42- | ||
| C. | NaHCO3═Na++H++CO32- | D. | NaHSO3$\frac{\underline{\;熔融\;}}{\;}$Na++H++SO42- |