��Ŀ����
����Ŀ�������������
��1���ؿ��к�����һ����Ԫ�ع��ɵĵ���A�뻯����B��������Ϊ232�������û���Ӧ������Ϊ��ɫ����C����һ����D������D��ˮ�����ڸ����¿ɵõ�B����
��i��д�����ɽ�������A��Ԫ�������ڱ��е�λ��Ϊ ��
��ii��д��D��ˮ������Ӧ�Ļ�ѧ����ʽ ��
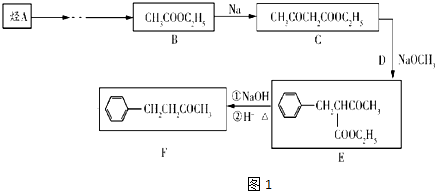
��2��ij��ú��ʯ��Ԥ������SiO2��63%����Al2O3��25%����Fe2O3��5%����������þ�Ļ�����ȣ�һ���ۺ����ù���������£� 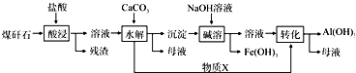
��i������X�Ļ�ѧʽΪ �� �����ܡ�ʱ��Ӧ�����ӷ���ʽΪ ��
��ii��Ϊ�ӿ조�����ʱ�����ʣ��ɲ�ȡ�Ĵ�ʩ�����ȣ��������ּ��ɣ�
��iii����֪Fe3+��ʼ�����ͳ�����ȫ��pH�ֱ�Ϊ2.1��3.2��Al3+��ʼ�����ͳ�����ȫ��pH�ֱ�Ϊ4.1��5.4��Ϊ�˻�ø����ƷAl��OH��3 �� ��ú��ʯ�������ȡҺ��ʼ����ֻ��CaCO3һ���Լ�������������ʵ�鷽���� ��
���𰸡�
��1���������ڢ�A�壻3Fe+4H2O ![]() Fe3O4+4H2
Fe3O4+4H2
��2��CO2��Al��OH��3+OH��=AlO2��+2H2O�����������Ũ�ȣ����߷�Ӧ�¶ȡ���Сú��ʯ������С����ֽ���ȣ�����CaCO3����pH��5.4�����˵õ�����
���������⣺��1���ؿ��к�����һ����Ԫ�ع��ɵĵ���A�뻯����B��������Ϊ232�������û���Ӧ������Ϊ��ɫ����C����һ����D������D��ˮ�����ڸ����¿ɵõ�B����AΪAl��BΪFe3O4 �� CΪFe��DΪAl2O3 �� ��i��AΪAl��A��Ԫ�������ڱ��е�λ��Ϊ�������ڢ�A�壬
���Դ��ǣ��������ڢ�A�壻 ��ii��DΪFe��D��ˮ������Ӧ�Ļ�ѧ����ʽΪ3Fe+4H2O ![]() Fe3O4+4H2 ��
Fe3O4+4H2 ��
���Դ��ǣ�3Fe+4H2O ![]() Fe3O4+4H2�� ��2����SiO2��63%����Al2O3��25%����Fe2O3��5%����������þ�Ļ�������������������ķ�ӦΪ��Al2O3+6H+�T2Al3++3H2O��Fe2O3+6H+�T2Fe3++3H2O������˵���ҺΪ�Ȼ������Ȼ�������Һ����̼���������Һ�е�������ʹ���������ӡ����������Ӷ�ˮ�������������������������ij����������ټ����������ƣ�ֻҪ���������ܽⷴӦΪ��Al��OH��3+OH���TAlO2��+2H2O��������ҺΪƫ��������Һ��ͨ�������̼��һ����Ӧ������������������i���Ȼ������Ȼ���ˮ�ⶼ�������ᣬ̼��ƺ����ᷴӦ�����Ȼ��ƺͶ�����̼����������X�Ƕ�����̼����������������������Һ��Ӧ���ɿ�����ƫ�����ƣ����ӷ�Ӧ����ʽΪ��Al��OH��3+OH��=AlO2��+2H2O��
Fe3O4+4H2�� ��2����SiO2��63%����Al2O3��25%����Fe2O3��5%����������þ�Ļ�������������������ķ�ӦΪ��Al2O3+6H+�T2Al3++3H2O��Fe2O3+6H+�T2Fe3++3H2O������˵���ҺΪ�Ȼ������Ȼ�������Һ����̼���������Һ�е�������ʹ���������ӡ����������Ӷ�ˮ�������������������������ij����������ټ����������ƣ�ֻҪ���������ܽⷴӦΪ��Al��OH��3+OH���TAlO2��+2H2O��������ҺΪƫ��������Һ��ͨ�������̼��һ����Ӧ������������������i���Ȼ������Ȼ���ˮ�ⶼ�������ᣬ̼��ƺ����ᷴӦ�����Ȼ��ƺͶ�����̼����������X�Ƕ�����̼����������������������Һ��Ӧ���ɿ�����ƫ�����ƣ����ӷ�Ӧ����ʽΪ��Al��OH��3+OH��=AlO2��+2H2O��
���Դ��ǣ�CO2��Al��OH��3+OH��=AlO2��+2H2O����ii������Ӱ�췴Ӧ���ʵ����ؿ�֪��Ϊ�ӿ조�����ʱ�����ʣ��ɲ�ȡ�Ĵ�ʩ�����������Ũ�ȡ����߷�Ӧ�¶ȡ���Сú��ʯ������С����ֽ���ȣ�
���Դ��ǣ����������Ũ�ȡ����߷�Ӧ�¶ȡ���Сú��ʯ������С����ֽ���ȣ���iii��Fe3+��ʼ�����ͳ�����ȫ��pH�ֱ�Ϊ2.1��3.2��Al3+��ʼ�����ͳ�����ȫ��pH�ֱ�Ϊ4.1��5.4��Ҫʹ��������ȫ�����������Ӳ�����������Һ��PHӦ��Ϊ3.2������������������ʱ������ҺpHΪ5.4����ʹ����������ȫ������
���Դ��ǣ�����CaCO3����pH��5.4�����˵õ�������

����Ŀ���� 2L �ݻ�������ܱ������ڣ�800��ʱ��Ӧ 2NO��g��+O2��g���T2NO2��g����ϵ�У�n��NO����ʱ��ı仯���±���
t/s | 0 | 1 | 2 | 3 | 4 | 5 |
n��NO��/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1����O2�ķ�Ӧ���ʱ�ʾ 0��2s �ڸ÷�Ӧ��ƽ����Ӧ���� v= �� ��������Ӧ��850���½��У���Ӧ2sʱ n��NO��=0.009mol�����Ҳ�����ʱ����ı䣬��÷�Ӧ���ȷ�Ӧ��
��2��ͼ�б�ʾNO2Ũ�ȱ仯��������������ĸ���� 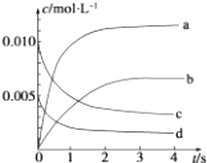
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����������ţ���
A.v��NO2��=2v��O2��
B.�����ڵ�ѹǿ���ֲ���
C.v����NO��=2v����O2��
D.�����������ܶȱ��ֲ���
��4����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����������ţ���
A.��ʱ�����NO2
B.�ʵ������¶�
C.����O2��Ũ��
D.ѡ���Ч������