题目内容
【题目】以下为从铝土矿(Al2O3、Fe2O3、泥沙)提取铝的流程图(注:整个流程中,不考虑泥沙的溶解及有关反应;C可以用来治疗胃酸过多):
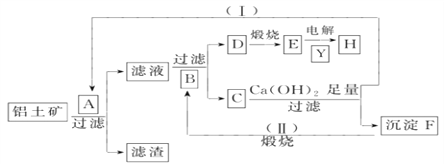
(1)A溶质的化学式___________;B的结构式____________,Y的名称_____________。
(2)写出①C与Ca(OH)2稀溶液反应的离子方程式: __________________________________。
②F→B的反应方程式: ______________________________。
(3)操作(Ⅰ)、(Ⅱ)在工业生产中的意义________________________。
【答案】 NaOH O=C=O 冰晶石 HCO3—+Ca++OH-===CaCO3↓+H2O CaCO3![]() CaO+CO2↑ (Ⅰ)、(Ⅱ)为工业原料的循环利用,使资源充分利用,可减少污染
CaO+CO2↑ (Ⅰ)、(Ⅱ)为工业原料的循环利用,使资源充分利用,可减少污染
【解析】C可以用来治疗胃酸过多,则C是碳酸氢钠,与足量氢氧化钙反应生成沉淀F为碳酸钙,A为氢氧化钠,铝土矿与氢氧化钠溶液反应时氧化铝溶解,生成偏铝酸钠和水,滤渣是氧化铁;碳酸钙高温分解生成B是CO2,通入滤液中与偏铝酸钠反应生成D为氢氧化铝沉淀和碳酸氢钠,氢氧化铝煅烧分解生成E是氧化铝,在冰晶石的作用下电解熔融的氧化铝生成铝,即H是Al,Y是冰晶石。
(1)根据以上分析可知A溶质的化学式为NaOH;B的结构式为O=C=O,Y的名称为冰晶石。(2)C与Ca(OH)2稀溶液反应的离子方程式为HCO3-+Ca++OH-=CaCO3↓+H2O。F→B的反应方程式为CaCO3![]() CaO+CO2↑。(3)根据转化关系图可知操作(Ⅰ)、(Ⅱ)在工业生产中的意义是为工业原料的循环利用,使资源充分利用,可减少污染。
CaO+CO2↑。(3)根据转化关系图可知操作(Ⅰ)、(Ⅱ)在工业生产中的意义是为工业原料的循环利用,使资源充分利用,可减少污染。
电解:化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识。它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法。解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等。例如本题中物质C是解答的突破口。

【题目】在2L的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为_______反应(选填吸热、放热)。
(2)能判断该反应是否达到化学平衡状态的依据是_______。
A.容器中压强不变 B.混合气体中 c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____℃。该温度下,若向该容器中充入n(CO2)=1mol, n(H2)=1mol,4min末达到平衡,CO2的转化率为_______;H2的体积分数为________________。
(4)写出增大逆反应速率的措施:___________________;(至少写两种)