题目内容
16.电池的发明是化学对人类的一项重大贡献,下列有关电池的叙述正确的是( )| A. | 锂离子电池已成为笔记本电脑、移动电话等低功耗电器的主流电源 | |
| B. | 氢氧燃料电池可将化学反应的热能直接转变为电能 | |
| C. | 铅蓄电池放电时铅在负极被氧化成二氧化铅 | |
| D. | 锌锰干电池工作一段时间后碳棒变细 |
分析 A、锂离子电池是二次电池,根据二次电池在生活中的使用以及二次电池的特点进行回答;
B、氢氧燃料电池是将化学能转化为电能的装置;
C、铅蓄电池放电时铅在负极被氧化成二价的铅离子;
D、根据锌锰干电池的正极是碳棒,该极上二氧化锰发生得电子的还原反应.
解答 解:A、锂离子电池是二次电池,且Li是最轻的金属,二次电池是可以连续充放电使用的电池,是目前手机、笔记本电脑等现代数码产品中应用最广泛的电池,故A正确;
B、氢氧燃料电池属于原电池的一种,是将化学能转化为电能的装置,不是将热能直接转变为电能,故B错误;
C、铅蓄电池放电时铅在负极被氧化成二价的铅离子,故C错误;
D、在锌锰干电池中,正极是碳棒,该极上二氧化锰发生得电子的还原反应,该电极质量不会减少,故D错误;
故选A.
点评 本题考查化学电源的有关知识,属于基本知识的考查,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
6.下列物质属于有机物的是( )
| A. | 氰化钾(KCN) | B. | 碳酸氢钾(KHCO3) | C. | 乙炔(C2H2) | D. | 碳化硅(SiC) |
7.容量瓶上需标有①压强 ②浓度 ③容量 ④温度 ⑤刻度线 五项中的( )
| A. | ①②④ | B. | ①③⑤ | C. | ②③⑤ | D. | ③④⑤ |
4.下列说法中不正确的是( )
| A. | 在原电池中,物质在负极发生氧化反应 | |
| B. | 在原电池中,电子由负极流向正极 | |
| C. | 在电解池中,物质在阳极发生还原反应 | |
| D. | 在电解池中,与电源负极相连的电极是阴极 |
1.25℃时,甲溶液的pH是10,乙溶液的pH是11,甲溶液与乙溶液中c(H+)之比是( )
| A. | 1:2 | B. | 2:1 | C. | 1:10 | D. | 10:1 |
8.下列离子方程式书写不正确的是( )
| A. | FeO溶于稀硝酸:FeO+2H+═Fe2++H2O | |
| B. | 醋酸与碳酸钙反应:2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2↑ | |
| C. | Ba(OH)2溶液与稀硫酸反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 往AlC13溶液中加入过量氨水:Al3++3 NH3•H2O═Al(OH)3↓+3NH4+ |
5.下列化学反应的离子方程式不正确的是( )
| A. | Na2S溶液中加入少量FeCl3溶液:2Fe3++S2-→2Fe2++S↓ | |
| B. | 向NaOH溶液中滴加碳酸氢钙溶液至OH-恰好完全反应:Ca2++2OH-+2HCO3-→CaCO3↓+2H2O+CO32- | |
| C. | 向NaClO溶液中通入少量SO2气体:ClO-+SO2+H2O→SO42-+Cl-+2H+ | |
| D. | Na2CO3溶液中滴入少量邻羟基苯甲酸溶液: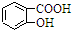 +CO32-→ +CO32-→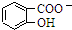 +HCO3- +HCO3- |
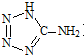 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.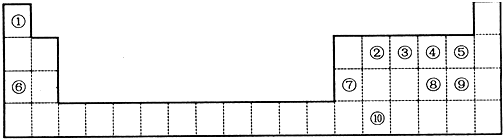
 ,元素②形成的最高价氧化物的结构式为O=C=O;
,元素②形成的最高价氧化物的结构式为O=C=O;