题目内容
【题目】丙烯是基本的有机化工原料,由丙烯经如下步骤可合成N异丙基丙烯酰胺,其可用于合成随温度变化的药物控制释放材料。
![]()
(1)丙烯的结构简式为___。
(2)反应Ⅰ的反应类型为___。
(3)反应Ⅱ___(填“能”或“不能”)用酸性KMnO4溶液作为氧化剂,理由是___。
(4)检验生成的B中是否含有A的方法是___;写出有关反应的化学方程式:___。
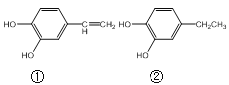
(5)M与A互称为同系物,相对分子质量比A大14,写出M所有可能的结构简式___。
(6)以B的钠盐作单体可以制成强吸水性树脂N,N属于___(填“线型”或“体型”)高分子材料,N的结构简式可表示为___。
(7)反应Ⅲ的另一种反应物的结构简式为___。
【答案】CH2=CHCH3 氧化反应 不能 酸性KMnO4溶液会将碳碳双键氧化 取适量生成的B先与一定量的NaOH溶液充分混合,再与适量新制氢氧化铜悬浊液共热,若产生砖红色沉淀,说明含有A,否则不含 CH2=CHCHO+2Cu(OH)2+NaOH![]() CH2=CHCOONa+Cu2O↓+3H2O
CH2=CHCOONa+Cu2O↓+3H2O 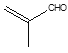 、
、![]() 、
、![]() 线型
线型 ![]()
【解析】
丙烯的结构为CH2=CHCH3,发生反应Ⅰ后生成A(CH2=CHCHO),因此反应Ⅰ即氧化反应;A再发生氧化反应生成B(CH2=CHCOOH),由于A中除醛基外还含有碳碳双键,因此在转化醛基时,要选择合适的氧化剂,防止碳碳双键也发生反应;最后由B生成C,对比C和B的结构差异,推测反应Ⅲ为取代反应,可能是B(CH2=CHCOOH)和2-丙胺在催化剂的作用下发生的反应。
(1)丙烯的结构简式即为CH2=CHCH3;
(2)通过分析可知,反应Ⅰ的反应类型为氧化反应;
(3)碳碳双键也可被酸性高锰酸钾溶液氧化,因此由A制备B的过程中,为了防止碳碳双键被氧化,不能选用酸性高锰酸钾溶液做氧化剂;
(4)A的结构中含有醛基,而B中没有,因此检验是否含有醛基即可;先将B与一定量的NaOH溶液混合,中和掉羧基,再加入适量的新制Cu(OH)2悬浊液,加热观察现象,若有砖红色沉淀出现,则含有A,若无则不含A;相关的方程式为:CH2=CHCHO+2Cu(OH)2+NaOH![]() CH2=CHCOONa+Cu2O↓+3H2O;
CH2=CHCOONa+Cu2O↓+3H2O;
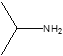
(5)由题可知,M的分子式比A的分子式中的碳原子数多1,M与A是同系物,所以M的结构可能有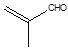 ,
,![]() ,
,![]() 三种;
三种;
(6)由题可知,N的结构为![]() ,属于线型高分子材料;
,属于线型高分子材料;
(7)通过分析可知,反应Ⅲ的另一种反应物为2-丙胺,结构简式为 。
。

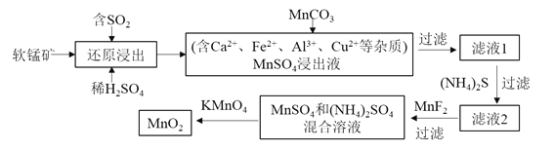
【题目】某同学探究Cu与NO的反应,查阅资料:①Cu与NO反应可生成CuO和N2,②酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
(1)实验室利用Cu和稀HNO3制备NO,写出反应的化学方程式_____________。
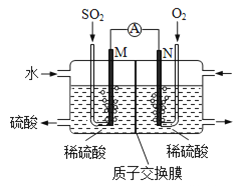
(2)选用如图所示装置完成Cu与NO的实验。(夹持装置略) 实验开始前,向装置中通入一段时间的N2。回答下列问题:
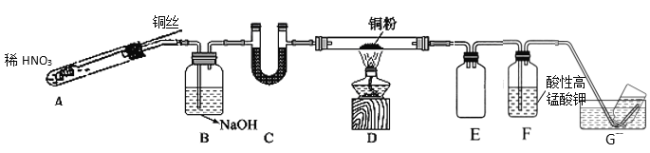
①使用铜丝的优点是_____________________装置E的作用为_______________。
②装置C中盛放的药品可能是_________;
③装置D中的现象是_______________;装置F中反应的离子方程式是_______________。
(3)测定NaNO2和NaNO3 混合溶液中NaNO2的浓度。 取25.00mL混合溶液于锥形瓶中,用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.90 | 20.12 | 20.00 | 19.88 |
①第一次实验数据出现异常,造成这种异常的原因可能是_________(填字母代号)。
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
d.酸性KMnO4溶液中含有其他氧化性试剂
e.锥形瓶洗净后用待测液润洗
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为___________________。
③NaNO2 的物质的量浓度为__________
【题目】下列根据实验操作和现象所得出的结论正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 等体积 | 相同时间内 |
|
B | 将湿润的淀粉- | 试纸只在 | 氧化性: |
C | 将光亮的镁条放入盛有 | 有大量气泡产生 | 生成的气体是 |
D | 向NaHCO3溶液中加入NaAlO2溶液 | 有白色沉淀生成 |
|
A. AB. BC. CD. D