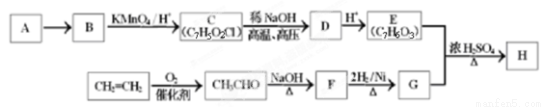
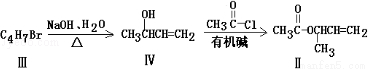
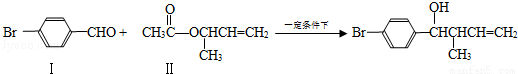题目内容
(15分)光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成。
(1)实验室常用来制备氯气的化学方程式为 ;
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(ΔH)分别为-890.3kJ·mol-1、-285.8kJ.mol-1和-283.0kJ.mol-1,则生成1m3(标准状况)CO所需热量为 ;
(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为
;
(4)COCl2的分解反应为COCl2(g)=Cl2(g)+CO(g) ΔH=+108kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出):
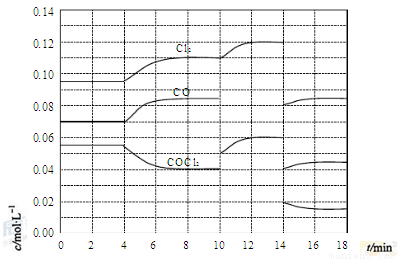
①计算反应在第8min时的平衡常数K= ;
②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2) T(8)
(填“<”、“>”或“=”),
③若12min时反应于温度T(8)下重新达到平衡,则此时c(COCl2)= mol·L-1;
④比较产物CO在2-3min、5-6min和12-13min时平均反应速率(平均反应速率分别以v(2-3)、v(5-6)、v(12-13))的大小 ;
⑤比较反应物COCl2在5-6min和15-16min时平均反应速率的大小:v(5-6) v(15-16)(填“<”、“>”或“=”),原因是 。

【解析】 (1)实验室中用二氧化锰与浓盐酸共热制取氯气。
(2)根据题目信息,写出CH4、H2、CO燃烧的热化学方程式分别为:
CH4(g)+2O2(g)= 2H2O (l)+CO2(g) ΔH1= —890.3kJ·moL-1 ①
H2(g)+1/2O2(g)= H2O (l) ΔH2= -285.8kJ·moL-1 ②
CO(g)+1/2O2(g)= CO2(g) ΔH3= -283.0kJ·moL-1 ③
工业用甲烷和二氧化碳反应制取CO的热化学方程式为:
CH4(g)+CO2(g)= 2H2(g)+2CO(g) ΔH
由盖斯定律和方程式①②③可知:
ΔH=ΔH1-2ΔH2-2ΔH3=(-890.3)kJ·moL-1-2×(-285.8)kJ·moL-1-2×(-283.0)kJ·moL-1=247.3 kJ·moL-1,即生成2mol CO,需要吸热247.3 KJ,那么要得到1立方米的CO,吸热为(1000/22.4)×247.3/2=5.52×103 KJ。
(4)①由图示可知8min时COCl2、Cl2、CO三种物质的浓度分别为0.04mol·L-1、0.11 mol·L-1、0.085 mol·L-1。所以此时其平衡常数为:0.11 mol·L-1×0.085 mol·L-1÷0.04 mol·L-1=0.23 4mol·L-1。②第8min时反应物的浓度比第2min时减小,生成物浓度增大,平衡向正反应方向移动。又因为正反应为吸热反应,所以T(2)>T(8)。④ 根据图像变化可知:在2min时升温, ⑤ 在10min时 增加COCl2的浓度,在12min时,反应达到平衡 。
【考点定位】热化学方程式的书写、反应热的计算、化学反应速率、影响化学反应速率的因素、化学平衡、化学图像。

[14分]已知:I2+2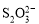

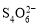 +2I―。相关物质的溶度积常数见下表:
+2I―。相关物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2?2H2O晶体,加入 调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=____________________;
过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2?2H2O晶体。
(2)在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,原因是_______________。(用化学方程式表示)。由CuCl2?2H2O晶体得到纯的无水CuCl2的合理方法是_______。
(3)某学习小组用“间接碘量法”测定含有CuCl2?2H2O晶体的试样(不含能与I―发生反应的氧化性质杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用___________作滴定指示荆,滴定终点的现象是_________________。
②CuCl2溶液与KI反应的离子方程式为______________________________。
③该试样中CuCl2?2H2O的质量百分数为___________________________。
现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第3周期元素的简单离子中半径最小 |
(1)画出元素T的原子结构示意图__________________________;
(2)元素Y与元素Z相比,金属性较强的是__________________(用元素符号表示),下列表述中能证明这一事实的是_________________(填序号);
a.Y单质的熔点比Z单质低b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式___________,并写出该化合物与水反应的离子方程式______;
(4)元素T和氢元素以原子个数比1∶1化合形成的化合物属于______________,元素Z与元素T形成的化合物属于____________________(以上两空选填“共价化合物”或“离子化合物”)。