题目内容
18.已知C3N4晶体具有比金刚石更大的硬度,且原子间均以单键结合.下列关于C3N4晶体的说法正确的是( )| A. | C3N4晶体是分子晶体 | |
| B. | C3N4晶体中C-N键长比金刚石中C-C要长 | |
| C. | C3N4晶体中每个碳原子连接4个氮原子,每个氮原子连接3个碳原子 | |
| D. | C3N4晶体中微粒间通过离子键结合 |
分析 C3N4晶体具有比金刚石更大的硬度,且原子间均以单键结合,说明该物质是原子晶体,每个C原子连接4个N原子、每个N原子连接3个C原子.
A.分子晶体熔沸点较低、硬度较小;
B.原子半径越大,原子间的键长越长;
C.该晶体中原子间均以单键结合,每个C原子能形成4个共价键、每个N原子能形成3个共价键;
D.离子晶体微粒之间通过离子键结合,原子晶体微粒之间通过共价键结合.
解答 解:C3N4晶体具有比金刚石更大的硬度,且原子间均以单键结合,说明该物质是原子晶体,每个C原子连接4个N原子、每个N原子连接3个C原子.
A.分子晶体熔沸点较低、硬度较小,原子晶体硬度较大,该晶体硬度比金刚石大,说明为原子晶体,故A错误;
B.原子半径越大,原子间的键长越长,原子半径C>N,所以C3N4晶体中C-N键长比金刚石中C-C要短,故B错误;
C.该晶体中原子间均以单键结合,且每个原子都达到8电子稳定结构,所以每个C原子能形成4个共价键、每个N原子能形成3个共价键,故C正确;
D.离子晶体微粒之间通过离子键结合,原子晶体微粒间通过共价键结合,该晶体是原子晶体,所以微粒间通过共价键结合,故D错误;
故选C.
点评 本题考查晶体类型判断、晶体结构等知识点,明确晶体类型判断方法、化学键类型判断方法及物质空间构型即可解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.据图判断下列说法正确的是( )


| A. | 图1中醋酸电离平衡常数:a点的比b点的小 | |
| B. | 图1中醋酸溶液的pH:a点的比b点的小 | |
| C. | 图2中c点对应的溶液为Fe(OH)3的不饱和溶液 | |
| D. | 由图2可知,欲除去CuSO4溶液中的Fe3+,可向溶液中加入CuO,调节pH约为4左右 |
6.下列化学措施不可行的是( )
| A. | 以 CH≡CH 和 HCl 反应制氯乙烯,进而制备聚氯乙烯塑料 | |
| B. | 浓氨水滴入生石灰中,将产生的气体通入 AlCl3溶液,可得到含AlO2-的溶液 | |
| C. | 使用催化剂不能改变工业合成 NH3 的反应限度 | |
| D. | 用浸有 KMnO4溶液的硅土来吸收水果释放的乙烯 |
13.下列说法中错误的是( )
| A. | 卤化氢中,以HF沸点最高,是由于HF分子间存在氢键 | |
| B. | 邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低 | |
| C. | N2分子中有一个σ键,2个π键 | |
| D. | 在元素周期表中,s区,d区和ds区的元素都是金属 |
3.下列物质中,不能使溴水和高锰酸钾酸性溶液褪色的是( )
| A. | C2H4 | B. | C3H6 | C. | C2H2 | D. | C3H8 |
10.一定温度下,某密闭容器中发生如下反应:A(g)+B(g)?C(g)+D(g)△H<0.当反应达到平衡时测得容器中各种物质均为amol.欲使C的平衡浓度增大一倍,在其他条件不变时,下列措施可采用的是( )
| A. | 降低温度 | B. | 恒容时,再通入2amolC和2amolD | ||
| C. | 恒压时,再通入2amolC和2amolD | D. | 恒容时,再通入amolA和amolB |
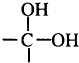 →
→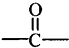 +H2O图中B和
+H2O图中B和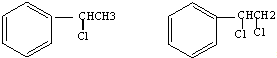 等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳(过程中一些小分子未写出).
等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳(过程中一些小分子未写出).
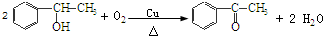 ’,该反应类型为氧化反应
’,该反应类型为氧化反应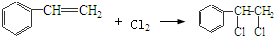 ,该反应类型为加成反应
,该反应类型为加成反应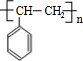
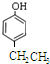 、
、 、
、