题目内容
【题目】(1)甲醇(CH3OH)是一种重要的化工原料。已知
CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ; △H = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ; △H = -566.00 kJ·mol-1
H2O(1) = H2O (g) ; △H = +44.00 kJ·mol-1
①试写出能表示CH3OH(l)燃烧热的热化学方程式:________________________________。试利用热化学方程式计算,完全燃烧16g甲醇生成CO2和H2O(l)时,放出的热量为__________kJ。
②科研人员新近开发出一种由甲醇和氧气以强碱做电解质溶液的新型手机电池。据此回答下列问题:氧气在________极反应;通入甲醇的电极反应式为________________________________。
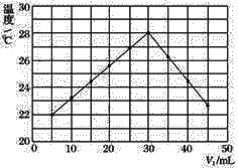
(2)800℃时A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,分析图像,回答下列问题:
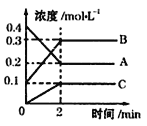
①该反应的方程式为_____________________________________________。
②2min内,用B表示的反应速率为__________________。
③下列能说明该反应达到平衡状态的是_______________。
A.体系压强保持不变 B.容器中气体密度保持不变
C.混合气体平均摩尔质量保持不变 D.每消耗2mol A的同时生成1mol C
E. A、B、C浓度之比为2:2:1 F.混合气体中A的质量分数保持不变
④为加快该反应的反应速率,可采取的措施是_______________。
A.恒容通入He B.分离出B C.选择高效的催化剂 D.适当升高体系温度
【答案】CH3OH(1)+![]() O2(g) = CO2(g) + 2H2O(1) △H= -814.64kJ·mol-1 407.32 正 CH3OH + 8OH--6e-= CO32-+ 6H2O 2A(g)
O2(g) = CO2(g) + 2H2O(1) △H= -814.64kJ·mol-1 407.32 正 CH3OH + 8OH--6e-= CO32-+ 6H2O 2A(g) ![]() 2B(g)+C(g) 0.1mol /(L·min) ACF CD
2B(g)+C(g) 0.1mol /(L·min) ACF CD
【解析】
(1) ① 甲醇燃烧热是1mol甲醇完全燃烧生成二氧化碳和液态水放出的能量;②氧气在正极得电子生成氢氧根离子;甲醇在负极失电子生成碳酸根离子;
(2) ① 根据图像,A的浓度降低,A是反应物;B、C的浓度升高,B、C是生成物;根据浓度的变化量比等于系数比书写方程式。②根据![]() 计算反应速率;③根据平衡标志判断;④根据影响反应速率的因素分析。
计算反应速率;③根据平衡标志判断;④根据影响反应速率的因素分析。
(1) ①Ⅰ、 CH3OH(1) + O2(g) = CO(g) + 2H2O(g);△H = -443.64kJ·mol-1
Ⅱ、2CO (g) + O2(g) = 2CO2(g);△H = -566.00 kJ·mol-1
Ⅲ、H2O(1) = H2O (g);△H = +44.00 kJ·mol-1
根据盖斯定律,Ⅰ+Ⅱ×![]() -Ⅲ×2得CH3OH(1)+
-Ⅲ×2得CH3OH(1)+![]() O2(g) = CO2(g) + 2H2O(1);△H= -814.64kJ·mol-1,根据热化学方程式,完全燃烧16g甲醇生成CO2和H2O(l)时,放出的热量为
O2(g) = CO2(g) + 2H2O(1);△H= -814.64kJ·mol-1,根据热化学方程式,完全燃烧16g甲醇生成CO2和H2O(l)时,放出的热量为![]() 814.64kJ·mol-1 =407.32kJ;
814.64kJ·mol-1 =407.32kJ;
②氧气得电子发生还原反应,所以氧气在正极通入,甲醇在负极失电子生成碳酸根离子,通入甲醇的电极反应式为CH3OH + 8OH--6e-= CO32-+ 6H2O;
(2) ① 根据图像,A的浓度降低,A是反应物;B、C的浓度升高,B、C是生成物;A的浓度变化是0.2mol/L、B的浓度变化是0.2mol/L、C的浓度变化是0.1mol/L,浓度的变化量比等于系数比,反应方程式是2A(g)![]() 2B(g)+C(g);
2B(g)+C(g);
②![]() =0.1mol/(L·min);
=0.1mol/(L·min);
③A. 反应2A(g)![]() 2B(g)+C(g),正反应气体系数和增大,压强是变量,体系压强保持不变,一定达到平衡状态,A正确;
2B(g)+C(g),正反应气体系数和增大,压强是变量,体系压强保持不变,一定达到平衡状态,A正确;
B.反应前后气体总质量不变、容器体积不变,密度是恒量,容器中气体密度保持不变,不一定平衡,B错误;
C. 反应前后气体总质量不变、气体物质的量减小,混合气体平均摩尔质量是变量,混合气体平均摩尔质量保持不变,一定达到平衡状态,C正确;
D.每消耗2mol A的同时生成1mol C,不能判断正逆反应速率是否相等,不一定达到平衡状态,D错误;
E. A、B、C浓度之比为2:2:1,浓度不一定不变,所以不一定达到平衡状态,E错误;
F.根据平衡定义,混合气体中A的质量分数保持不变,一定达到平衡状态,F正确;
故选ACF;
④A.恒容通入He ,浓度不变,反应速率不变,A错误;
B.分离出B,浓度减小,反应速率减慢,B错误;
C.选择高效的催化剂,能加快反应速率,C正确;
D.适当升高体系温度,反应速率一定加快,D正确;
故选CD。

 全优点练单元计划系列答案
全优点练单元计划系列答案