题目内容
【题目】已知25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=5.0×10-13。该温度下,下列说法错误的是
A. AgCl的悬浊液中通入少量HCl,c(Ag+)减小
B. AgCl和AgBr共存的悬浊液中,c(Cl-)/c(Br-)=360
C. AgBr悬浊液中加入足量NaCl可能有AgCl沉淀生成
D. 等浓度的NaCl和NaBr混合溶液中滴加AgNO3溶液,先析出AgCl沉淀
【答案】D
【解析】试题分析:A.AgCl的悬浊液中通入少量HCl,溶解平衡向逆反应方向进行,c(Ag+)减小,A正确;B.AgCl和AgBr共存的悬浊液中,c(Cl-)/c(Br-)=![]() =360,B正确;C.只要溶液c(Ag+)·c(Cl-)>Ksp(AgCl)即可产生氯化银沉淀,因此AgBr悬浊液中加入足量NaCl可能有AgCl沉淀生成,C正确;D.由于氯化银和溴化银的组成相似,且溴化银的溶度积常数小于氯化银,所以等浓度的NaCl和NaBr混合溶液中滴加AgNO3溶液,先析出AgBr沉淀,D错误,答案选D。
=360,B正确;C.只要溶液c(Ag+)·c(Cl-)>Ksp(AgCl)即可产生氯化银沉淀,因此AgBr悬浊液中加入足量NaCl可能有AgCl沉淀生成,C正确;D.由于氯化银和溴化银的组成相似,且溴化银的溶度积常数小于氯化银,所以等浓度的NaCl和NaBr混合溶液中滴加AgNO3溶液,先析出AgBr沉淀,D错误,答案选D。

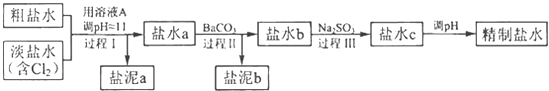
【题目】工业上用难溶于水的碳酸锶(SrCO3)粉末为原料(含少量钡和铁的化合物)制备高纯六水氯化锶晶体(SrCl26H2O),其过程为: 
已知:Ⅰ.有关氢氧化物沉淀的pH:
氢氧化物 | Fe(OH)3 | Fe(OH)2 |
开始沉淀的pH | 1.5 | 6.5 |
沉淀完全的pH | 3.7 | 9.7 |
Ⅱ.SrCl26H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水.
(1)操作①中碳酸锶与盐酸反应的离子方程式 .
(2)在步骤②﹣③的过程中,将溶液的pH值由1调节至;宜用的试剂为 . A.1.5 B.3.7 C.9.7 D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体
(3)操作②中加入H2O2发生反应的离子方程式是 .
(4)操作③中所得滤渣的主要成分是(填化学式).
(5)工业上用热风吹干六水氯化锶,适宜的温度是 .
A.50~60℃
B.80~100℃
C.100℃以上
(6)步骤⑥宜选用的无机洗涤剂是 .
【题目】在1.0L密闭容器中放入0.10mol A(g),在一定温度进行如下反应:A(g)═B(g)+C(g)△H=+85.1kJmol﹣1反应时间(t)与容器内气体总压强(p)的数据见表:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为(写出两项措施).
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为 . 平衡时A的转化率为 , 列式并计算反应的平衡常数K .
(3)由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n(总)=mol,n(A)=mol.