题目内容
下列离子方程式正确的是
| A.等物质的量的Ba(OH)2与KAl(SO4)2·12H2O溶液混合: 3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓ |
| B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C.H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2↑ |
| D.CuCl2溶液中加入NaHS溶液:Cu2++2HS-+2H2O=Cu(OH)2↓+2H2S↑ |
A
解析试题分析:B.Fe3+有强的氧化性会和碘离子发生氧化还原反应,错误;C.氧气中没有18O2生成,错误;D.CuCl2溶液中加入NaHS溶液生成了CuS沉淀,错误;
考点:本题考查了离子方程式的判断。

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
下列示意图与对应的反应情况符合的是( )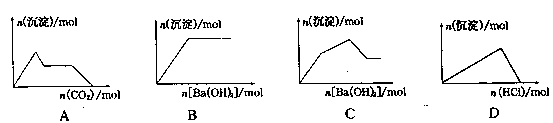
| A.向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量 |
| B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量 |
| C.向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量 |
| D.向NaAlO2溶液中逐滴加入盐酸至过量 |
将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述不正确的是( )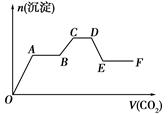
| A.O~A段反应的化学方程式是Ba(OH)2+CO2=BaCO3↓+H2O |
| B.B~C段反应的离子方程式是2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32- |
| C.A~B段与C~D段所发生的反应相同 |
| D.D~E段沉淀的减少是由于碳酸钡固体的消失所致 |
某溶液可能含有Cl-、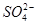 、
、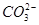 、NH+ 4、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
、NH+ 4、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
| A.NH+ 4Fe3+一定存在, K+可能存在 |
| B.Cl?一定存在,且c(Cl?)≤0.4 mol/L |
C.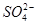 、NH+ 4Fe3+一定存在,且物质的量浓度均为0.02 mol/L 、NH+ 4Fe3+一定存在,且物质的量浓度均为0.02 mol/L |
D.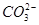 、Al3+一定不存在,K+一定存在 、Al3+一定不存在,K+一定存在 |
下列离子方程式正确的是 ( )
| A.NH4HCO3溶液与过量NaOH溶液反应:NH 4++ OH―=NH3↑+ H2O |
B.用惰性电极电解饱和氯化钠溶液:2Cl― + 2H +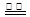 H2↑+ Cl2↑ H2↑+ Cl2↑ |
| C.向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I―= 2Fe2++I2 |
| D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32― + 6H+ + 2MnO4―=5SO42― + 2Mn2+ +3H2O |
下列物质中含有自由移动的Cl―的是( )
| A.KClO3溶液 | B.液态HCl |
| C.KCl溶液 | D.NaCl晶体 |
在水溶液中能大量共存,且加入过量稀硫酸时,有气体生成的是( )
| A.Na+、Ag+、CO32-、Cl- | B.K+、Ba2+、SO42-、Cl- |
| C.Na+、K+、CO32-、Cl- | D.Na+、K+、Cl-、SO42- |
下列反应的离子方程式书写正确的是( )
| A.钠和冷水反应Na+2H2O=Na++2OH-+H2↑ |
| B.金属铝溶于氢氧化钠溶液Al+2OH-=AlO2-+H2↑ |
| C.金属铝溶于盐酸中2Al+6H+=2Al3++3H2↑ |
| D.铁跟稀硫酸反应2Fe+6H+=2Fe3++3H2↑ |
下列离子方程式,正确的是
| A.氢氧化铁与盐酸反应:H++OH-=H2O |
| B.过量NaHSO4溶液与少量Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| C.铁与H2SO4反应:Fe+2H+=Fe3++H2↑ |
| D.CaCO3溶于稀盐酸中:CO32-+2H+=CO2↑+H2O |