题目内容
【题目】下列实验操作中都正确的选项是 ( )
①用剩的药品为避免浪费应放回原瓶
②蒸发氯化钠溶液时要用玻璃棒不断搅拌
③称取易潮解的药品必须放在玻璃器皿中称量
④浓硫酸的稀释时,将水沿烧杯内壁缓缓倒入,并不断搅拌
A.②③B.②③④C.②④D.①②③④
【答案】A
【解析】
:①一般用剩后的药品不能放回原瓶,防止试剂污染,特殊药品如钠等需要放回原瓶,故错误;
②蒸发时防止局部温度过高,则要用玻璃棒不断搅动,故正确;
③易潮解的药品时,不能直接接触托盘,必须放在玻璃器皿中称量,故正确;
④浓硫酸稀释时因稀释放热应将浓硫酸倒入水中,故错误;
正确的有②③,故答案为A。

练习册系列答案
相关题目
【题目】下表所列各组物质中,物质之间能通过一步反应实现如图所示转化的是
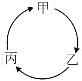
物质 选项 | 甲 | 乙 | 丙 |
A | SO2 | SO3 | H2SO4 |
B | NH4Cl | NH3 | NO |
C | Na2O | NaCl | NaOH |
D | Al(OH)3 | Al2O3 | AlCl3 |
A. A B. B C. C D. D