题目内容
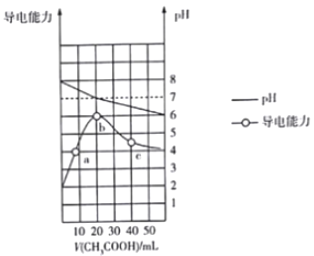
【题目】298K时向20mL0.1mol·L-1MOH 溶液中滴加0.1mol·L-1CH3COOH溶液,所得溶液的pH 及导电能力变化如图所示,下列叙述正确的是( )
A. MOH 是强电解质
B. b点对应的盐不水解
C. c 点溶液中:c(CH3COO-)>c(M+)>c(H+)>c(OH-)
D. a 点溶液中:c(OH-)+c(CH3COO-)+)+c(M+)
【答案】C
【解析】试题分析:由图像可知,0.1mol·L-1MOH溶液的pH为8而不是13,说明MOH是弱碱,故其为弱电解质。在a点溶液中有OH-、CH3COO-、H+、M+等4种离子,由电荷守恒可知,OH-)+c(CH3COO-)=c(H+)+c(M+)。在b点,两者恰好完全反应生成弱酸弱碱盐CH3COOM,该盐水解后溶液的pH=6,溶液显弱酸性,说明M+的水解程度大于CH3COO-的水解程度,所以在b点溶液中c(CH3COO-)>c(M+)>c(H+)>c(OH-)。在c点,醋酸过量使溶液酸性增强,依据电荷守恒可以判断,溶液中c(CH3COO-)>c(M+)>c(H+)>c(OH-)。在一定温度下,水的离子积是定值,其值不随溶液的pH变化而变化。综上所述,C正确,本题选C。

 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案【题目】硫代硫酸钠晶体(Na2S2O3·5H2O)又称海波,呈无色透明状,易溶于水,不溶于乙醇,常用作棉织物漂白后的脱氯剂、定量分析中的还原剂。
Ⅰ. Na2S2O3·5H2O的制备
Na2S2O3·5H2O的制备方法有多种,其中亚硫酸钠法是工业和实验室中的主要方法:
Na2SO3+S+5H2O![]() Na2S2O3·5H2O
Na2S2O3·5H2O
制备过程如下:
①称取12.6gNa2SO3于100mL烧杯中,加50mL去离子水搅拌溶解。
②另取4.0g硫粉于200mL烧杯中,加6mL乙醇充分搅拌均匀将其润湿,再加入Na2SO3溶液,隔石棉网小火加热煮沸,不断搅拌至硫粉几乎全部反应。
③停止加热,待溶液稍冷却后加2g活性炭,加热煮沸2分钟(脱色)。
④趁热过滤,得滤液至蒸发皿中,_________________、____________________。
⑤过滤、洗涤,用滤纸吸干后,称重,计算产率。
(1)加入的硫粉用乙醇润湿的目的是____________________________。
(2)步骤④趁热过滤的原因_____________________,空格处应采取的操作是_________________、____________________。
(3)步骤⑤洗涤过程中,为防止有部分产品损失,应选用的试剂为__________________________。
(4)滤液中除Na2S2O3 和未反应完全的Na2SO3外,最可能存在的无机杂质是________________,生成该杂质的原因可能是____________________________。
Ⅱ.产品纯度的测定
准确称取1.00g产品(硫代硫酸钠晶体的摩尔质量为248g/mol),用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol/LI2的标准溶液滴定,反应的离子方程式为:2S2O32-+I2=S4O62-+2I-,记录数据如下:
滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
1 | 0.30 | 21.32 |
2 | 0.36 | 22.56 |
3 | 0.10 | 21.08 |
(5)计算所得产品的纯度为___________(保留三位有效数字),该数据的合理解释可能是__________(不考虑实验操作引起的误差)。
Ⅲ.产品的应用
(6)Na2S2O3 常用于脱氯剂,在溶液中易被Cl2 氧化为SO42-,该反应的离子方程式为 _____________________________。