��Ŀ����
����Ŀ������˵����ȷ���ǣ�������
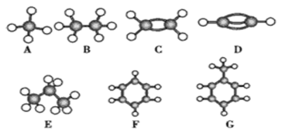
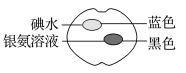
A.��ϩ������ϩ����Ȳ������Ȳ����ʹ��ˮ����������Һ��ɫ�����������Լ�������Ӧ�ķ�Ӧ�����Dz�ͬ��
B.��ķ����廯�����DZ����������������
C.�����±���Һ�塢���ۻ�Ϸ�Ӧ���ɵ���״�л���ʺ��ɫ������������������������ɵ�
D.�����������ᣨTCCA��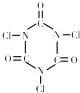 ��������Ӿ�صȹ������������ĵ�������Ʒ������ǿ�ҵ������̼�ζ������Ч����90%���ϣ��ṹ��ʽ��ͼ��ʾ���ݴ��Ʋ�TCCA��������Ԫ��������
��������Ӿ�صȹ������������ĵ�������Ʒ������ǿ�ҵ������̼�ζ������Ч����90%���ϣ��ṹ��ʽ��ͼ��ʾ���ݴ��Ʋ�TCCA��������Ԫ��������
���𰸡�D
��������
A������ϩ����̼̼�����ͼ���û��ϩ�����ʣ����Ծ���ϩ���岻�ܷ����ӳɷ�Ӧ��Ҳ���ܱ����Ը��������Һ���������Ծ���ϩ����ʹ��ˮ�����Ը��������Һ��ɫ��A�����
B���ӷ��ӽṹ�Ͽ�������ɶ���Ϊ���ǻ�ȩ�����ǻ�ͪ�����ǵ���ˮ��������������ڵ��ǣ�������������ǣ�B�����
C���屽�ͱ����廥�ܣ������ڱ����屽��ʹ��Һ�ʺ��ɫ��C�����
D�����л��ﻯѧʽΪC3O3N3Cl3�����л������ʻ�CΪ+4�ۡ�OԪ��Ϊ��2�ۡ��ļ���NԪ��Ϊ��3�ۣ���ClԪ�ػ��ϼ�Ϊx�����ݻ��ϼ۴�����Ϊ0ȷ��ClԪ�ػ��ϼۣ�![]() �ۣ�D����ȷ��
�ۣ�D����ȷ��
��ѡD��

����Ŀ��FeCl3����Ҫ�Ļ���ԭ�ϣ���ˮ�Ȼ�����300��ʱ���������׳��⡣
I���Ʊ���ˮ�Ȼ�����
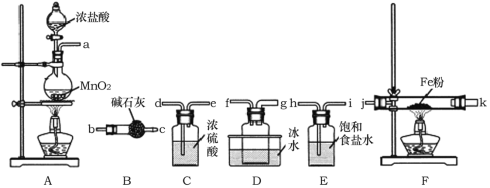
��1��Aװ���з�����Ӧ�����ӷ���ʽΪ______________��
��2��װ�õ�����˳��Ϊa��______________��j��k��______________��������������Сд��ĸ��ʾ����
��3��ʵ�������ȡ����Fװ�ò������еĹ����ˮ�ܽ⣬����⣬������Һ�к���Fe2+������ԭ��Ϊ______________��
II��̽��FeCl3��SO2�ķ�Ӧ��
��4����֪��Ӧ��ϵ�д����������ֻ�ѧ�仯��
��i��Fe3+��SO2������Ϸ�Ӧ����Fe(SO2)63+������ɫ����
��ii��Fe3+��SO2����������ԭ��Ӧ�������ӷ���ʽΪ______________��
��5��ʵ�鲽�����£�������������
���� | ���� | ���� |
��ȡ5mL1mol��L-1FeCl3��Һ���Թ��У�ͨ��SO2�����͡� | ��Һ�ܿ��ɻ�ɫ��Ϊ����ɫ | |
���ü�������䲽����еĺ���ɫҺ�塣 | _______________ | ����ɫҺ�岻��Fe(OH)3���� |
�۽�������е���Һ���á� | 1Сʱ����Һ��Ϊdz��ɫ | |
�����������Һ����2��___________ ��Һ(�ѧʽ)�� | _______________ | ��Һ�к���Fe2+ |
��6��������ʵ���֪����Ӧ��i������ii���Ļ�ܴ�С��ϵ�ǣ�E(i)________E(ii)������>������<������=������ͬ����ƽ�ⳣ����С��ϵ�ǣ�K(i)__________K(ii)��
����Ŀ��һ���¶��£��������ݻ���ͬ�ĺ����ܱ������а���ͬ��ʽͶ�뷴Ӧ�������Ӧ2SO2(g)+ O2(g) ![]() 2SO3(g)(����Ӧ����)����÷�Ӧ������������£�
2SO3(g)(����Ӧ����)����÷�Ӧ������������£�
����1 | ����2 | ����3 | |
��Ӧ�¶�T/K | 700 | 700 | 800 |
��Ӧ��Ͷ���� | 2molSO2��1molO2 | 4molSO3 | 2molSO2��1molO2 |
ƽ��v��(SO2)/mol��L-1��s-1 | v1 | v2 | v3 |
ƽ��c(SO3)/mol��L-1 | c1 | c2 | c3 |
ƽ����ϵ��ѹǿp/Pa | p1 | p2 | p3 |
���ʵ�ƽ��ת����a | ��1 (SO2) | ��2 (SO3) | ��3 (SO2) |
ƽ�ⳣ��K | K1 | K2 | K3 |
����˵����ȷ����
A. v/span>1<v2��c2< 2c1 B. K1>K3��p2> 2p3
C. v1<v3����1(SO2) <��3(SO2) D. c2> 2c3����2(SO3)+��3(SO2)<1