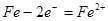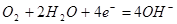题目内容
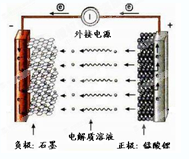
(10分)下列所示的装置中A为Zn,B为Cu,C、D均为碳棒。
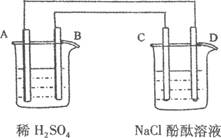
则(1)A发生了____反应(填氧化或还原).C为____极。
(2)D极周围溶液中的现象____________________________________
原因是__________________________________________
(3)当A电极上的金属质量减少1.3g,则C电极上产生气体在标准状况下的体积为_________________________L。

则(1)A发生了____反应(填氧化或还原).C为____极。
(2)D极周围溶液中的现象____________________________________
原因是__________________________________________
(3)当A电极上的金属质量减少1.3g,则C电极上产生气体在标准状况下的体积为_________________________L。
(1)阳(1分) 氧化(1分)(2)溶液变红(2分)由于H+放电,水
的电离平衡发生移动,使D极周围的溶液中pH>7,溶液显碱性,使酚酞变红。(3分)
(3)0.448(3分)
的电离平衡发生移动,使D极周围的溶液中pH>7,溶液显碱性,使酚酞变红。(3分)
(3)0.448(3分)
(1)根据装置特点可知,左侧是原电池,右侧是电解池。锌比铜活泼,所以锌是负极,失去电子,发生氧化反应。铜是正极,溶液中的氢离子在正极得到电子。C接电源的正极,因此C是阳极。
(2)D是阴极,溶液中的氢离子在阴极放电,生成氢气。由于H+放电,水的电离平衡发生移动,使D极周围的溶液中pH>7,溶液显碱性,使酚酞变红。
(3)A是锌失去电子,则转移电子是1.3g÷65g/mol×2=0.04mol。C是氯离子放电,产生氯气。根据电子得失守恒可知,生成氯气是0.02mol,标准状况下的体积是0.02mol×22.4L/mol=0.448L。
(2)D是阴极,溶液中的氢离子在阴极放电,生成氢气。由于H+放电,水的电离平衡发生移动,使D极周围的溶液中pH>7,溶液显碱性,使酚酞变红。
(3)A是锌失去电子,则转移电子是1.3g÷65g/mol×2=0.04mol。C是氯离子放电,产生氯气。根据电子得失守恒可知,生成氯气是0.02mol,标准状况下的体积是0.02mol×22.4L/mol=0.448L。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 LiMnO4+C。
LiMnO4+C。