题目内容
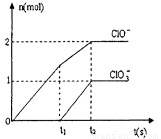
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示。已知,生成
试回答:
(1)t2时,Ca(ClO)2与Ca(ClO3)2的物质的量之和为_________ mol,该石灰乳中含有的Ca(OH)2的质量是_________ g。
(2)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入氯气的速率不同,n(ClO-)和n (![]() )的比例也不同。若在原石灰乳中通入氯气的速率加快,则反应后
)的比例也不同。若在原石灰乳中通入氯气的速率加快,则反应后![]() _____2(填“>”“<”或“=”)。
_____2(填“>”“<”或“=”)。
(3)若![]() =a,则n(Cl-)=_________ mol(用含a的代数式表示)。
=a,则n(Cl-)=_________ mol(用含a的代数式表示)。
(1)3 740
(2)<
(3)a·n(![]() )+5
)+5
解析:(1)由图知,Ca(ClO)2与Ca(ClO3)2的物质的量之和为3 mol,根据得失电子守恒得CaCl2为7 mol,故Ca(OH)2的质量为(3 mol+7 mol)×
(2)通入氯气的速率加快,反应速率加快,反应放出的热量无法很快散失,体系温度升高,生成的n(![]() )增多。
)增多。

练习册系列答案
相关题目
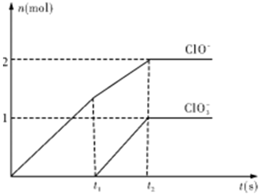 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、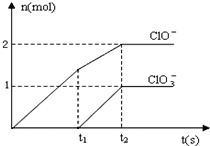 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示. (2013?江西模拟)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、
(2013?江西模拟)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、