题目内容
现有X、Y、Z、M四种元素均为短周期元素.有关信息如下表:
(1)X元素在周期表中第______周期、第______族;
(2)Y元素的元素符号为______,1个单质分子中含______个共用电子对;
(3)Z能在CO2气体中燃烧,其化学反应方程式为______.
(4)化合物X2M3中,各原子(或离子)最外层均达到8电子稳定结构,则X2M3的电子式为______,该化合物的水溶液在空气中久置后会被氧化而变质,生成一种单质,所得溶液呈强碱性.用化学方程式表示这个变化过程______.
| 原子或分子结构、单质或化合物相关信息 | |
| X | 含X元素的物质焰色反应为黄色 |
| Y | 单质为双原子分子.若低温蒸发液态空气,因其沸点较低可先获得Y的单质 |
| Z | Z元素原子易失去2个电子形成8电子结构的离子 |
| M | M元素原子的最外层电子数是K层电子数的3倍,M与X处于同一周期 |
(2)Y元素的元素符号为______,1个单质分子中含______个共用电子对;
(3)Z能在CO2气体中燃烧,其化学反应方程式为______.
(4)化合物X2M3中,各原子(或离子)最外层均达到8电子稳定结构,则X2M3的电子式为______,该化合物的水溶液在空气中久置后会被氧化而变质,生成一种单质,所得溶液呈强碱性.用化学方程式表示这个变化过程______.
X、Y、Z、M四种元素均为短周期元素,含X元素的物质焰色反应为黄色,则X为Na;Y单质为双原子分子,若低温蒸发液态空气,因其沸点较低可先获得Y的单质,则Y为N元素;Z元素原子易失去2个电子形成8电子结构的离子,则Z为Mg;M元素原子的最外层电子数是K层电子数的3倍,最外层电子数为6,M与X处于同一周期,则M为S元素,
(1)X为Na元素,在周期表中第三周期第ⅠA族,故答案为:三;ⅠA;
(2)Y为N元素,1个单质分子中含3个共用电子对,故答案为:N;3;
(3)Mg在CO2气体中燃烧生成MgO与C,其化学反应方程式为2Mg+CO2
2MgO+C,
故答案为:2Mg+CO2
2MgO+C;
(4)化合物Na2S3中,各原子(或离子)最外层均达到8电子稳定结构,应是离子化合物,S32-离子中S原子形成1对共用电子对,其电子式为: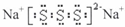 ,该化合物的水溶液在空气中久置后会被氧化而变质,生成一种单质,所得溶液呈强碱性,生成NaOH与S,用化学方程式表示这个变化过程为:2Na2S3+O2+2H2O=4NaOH+6S,故答案为:
,该化合物的水溶液在空气中久置后会被氧化而变质,生成一种单质,所得溶液呈强碱性,生成NaOH与S,用化学方程式表示这个变化过程为:2Na2S3+O2+2H2O=4NaOH+6S,故答案为: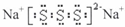 ;2Na2S3+O2+2H2O=4NaOH+6S.
;2Na2S3+O2+2H2O=4NaOH+6S.
(1)X为Na元素,在周期表中第三周期第ⅠA族,故答案为:三;ⅠA;
(2)Y为N元素,1个单质分子中含3个共用电子对,故答案为:N;3;
(3)Mg在CO2气体中燃烧生成MgO与C,其化学反应方程式为2Mg+CO2
| ||
故答案为:2Mg+CO2
| ||
(4)化合物Na2S3中,各原子(或离子)最外层均达到8电子稳定结构,应是离子化合物,S32-离子中S原子形成1对共用电子对,其电子式为:
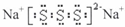 ,该化合物的水溶液在空气中久置后会被氧化而变质,生成一种单质,所得溶液呈强碱性,生成NaOH与S,用化学方程式表示这个变化过程为:2Na2S3+O2+2H2O=4NaOH+6S,故答案为:
,该化合物的水溶液在空气中久置后会被氧化而变质,生成一种单质,所得溶液呈强碱性,生成NaOH与S,用化学方程式表示这个变化过程为:2Na2S3+O2+2H2O=4NaOH+6S,故答案为: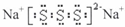 ;2Na2S3+O2+2H2O=4NaOH+6S.
;2Na2S3+O2+2H2O=4NaOH+6S.
练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目