��Ŀ����
����Ŀ���������ƣ�![]() ����дΪNaA�����������ϵķ��������о����������ᣨHA�����־�������������A�C����֪25 ��ʱ��HA��Ka=6.25��10�C5��H2CO3��Ka1=4.17��10�C7��Ka2=4.90��10�C11��������̼�����ϵĹ����У���������NaA�⣬�����ѹ����CO2���塣����˵����ȷ���ǣ��¶�Ϊ25���������������������ɷ֣�
����дΪNaA�����������ϵķ��������о����������ᣨHA�����־�������������A�C����֪25 ��ʱ��HA��Ka=6.25��10�C5��H2CO3��Ka1=4.17��10�C7��Ka2=4.90��10�C11��������̼�����ϵĹ����У���������NaA�⣬�����ѹ����CO2���塣����˵����ȷ���ǣ��¶�Ϊ25���������������������ɷ֣�
A�������δ��CO2�����ϣ�̼�����ϵ��־������ϵ�
B�����CO2����ѹ����������c(A�C)����
C����pHΪ5.0ʱ��������![]() =0.16
=0.16
D��̼�������и������ӵ�Ũ�ȹ�ϵΪ��c(H+)=c(![]() )+c(
)+c(![]() )+c(OH�C)�Cc(HA)
)+c(OH�C)�Cc(HA)
���𰸡�C
��������
���������A���������⣬�����ᣨHA�����־�������������A�C�������δ��CO2�����ϣ�̼�����ϵ��־������ϸߣ�A�����B�����CO2����ѹ����CO2+H2O+A![]() HA+HCO3-��ƽ�����ƣ�������c(A�C)��С��B�����C����pHΪ5.0ʱ��������
HA+HCO3-��ƽ�����ƣ�������c(A�C)��С��B�����C����pHΪ5.0ʱ��������![]() =c(H+)��Ka=10-5����6.25��10�C5��=0.16,C����ȷ��D�����ݵ���غ��c(H+)+c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)+c(A-)�����������غ��c(Na+)=c(A-)+c(HA)����ʽ��������ȥc(Na+)��c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)-c(HA)����D�����ѡC��
=c(H+)��Ka=10-5����6.25��10�C5��=0.16,C����ȷ��D�����ݵ���غ��c(H+)+c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)+c(A-)�����������غ��c(Na+)=c(A-)+c(HA)����ʽ��������ȥc(Na+)��c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)-c(HA)����D�����ѡC��

����Ŀ�����������Fe��ȥ��ˮ���е������Σ�NO3-���ѳ�Ϊ�������о����ȵ�֮һ��
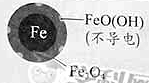
��1��Fe��ԭˮ����NO3-�ķ�Ӧԭ����ͼ��ʾ��

����������������________��
�������ĵ缫��Ӧʽ��_________��
��2������������Ͷ��ˮ���У���24Сʱ�ⶨNO3����ȥ���ʺ�pH��������£�
��ʼpH | pH=2.5 | pH=4.5 |
NO3����ȥ���� | �ӽ�100% | ��50% |
24СʱpH | �ӽ����� | �ӽ����� |
��������������̬ |
|
|
pH=4.5ʱ��NO3����ȥ���ʵ͡���ԭ����________��
��3��ʵ�鷢�֣��ڳ�ʼpH=4.5��ˮ����Ͷ���������۵�ͬʱ������һ������Fe2+�����������NO3����ȥ���ʡ���Fe2+������������ּ��裺
��. Fe2+ֱ�ӻ�ԭNO3����
��. Fe2+�ƻ�FeO��OH�������㡣
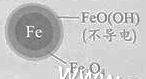
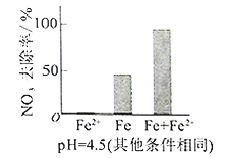
�����Ա�ʵ�飬�����ͼ��ʾ���ɵõ��Ľ�����_______��
��ͬλ��ʾ�ٷ�֤ʵFe2+����FeO��OH����Ӧ����Fe3O4����ϸ÷�Ӧ�����ӷ���ʽ�����ͼ���Fe2+���NO3��ȥ���ʵ�ԭ��______��
��4�����������루2����ͬ����1Сʱ�ⶨNO3����ȥ���ʺ�pH��������£�
��ʼpH | pH=2.5 | pH=4.5 |
NO3����ȥ���� | Լ10% | Լ3% |
1СʱpH | �ӽ����� | �ӽ����� |
�루2�������ݶԱȣ����ͣ�2���г�ʼpH��ͬʱ��NO3��ȥ���ʺ���������������̬��ͬ��ԭ��__________��
����Ŀ������ѡ�����ܷ�����ѧ��Ӧ���Ҽ���Ϊȡ����Ӧ������Ϊ�ӳɷ�Ӧ���ǣ� ��
�� | �� | |
A | ������ˮ | ��ϩ��ˮ���Ҵ��������� |
B | ��֬ˮ�� | �������������������ȣ� |
C | �������������ڹ������� | ������Ҵ���������Ӧ�����������ȣ� |
D | ��ϩ��������Ȼ�̼��Һ | �Ҵ����Ʒ�Ӧ |