题目内容
(4分)下图是实验室制取溴苯的装置:
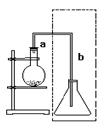
导管a段的作用 。反 应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。
应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。

导管a段的作用 。反
 应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。
应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。冷凝回流、导气,防倒吸
略

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
题目内容

 应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。
应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案