题目内容
【题目】下列描述中正确的是( )
A.![]() 为V形的极性分子
为V形的极性分子
B.ClO3-的空间构型为平面三角形
C.SF6中有7对完全相同的成键电子对
D.SiF4和SO32-的中心原子均为sp3杂化
【答案】D
【解析】
A. CS2的中心原子C的价层电子对数=2+![]() (4-2×2)=2,孤电子对数为0,因此几何构型为直线型,结构对称,正负电荷的中心重合,为非极性分子,故A错误;
(4-2×2)=2,孤电子对数为0,因此几何构型为直线型,结构对称,正负电荷的中心重合,为非极性分子,故A错误;
B. ClO3-中Cl的价层电子对数=3+![]() (7+1-3×2)=3+1=4,含有一个孤电子对,则离子的空间构型为三角锥形,故B错误;
(7+1-3×2)=3+1=4,含有一个孤电子对,则离子的空间构型为三角锥形,故B错误;
C. SF6中一个S-F键含有一个成键电子对,SF6中含有6个S-F键,则分子中有6对完全相同的成键电子对,故C错误;
D. SiF4中Si的价层电子对数=4+![]() (4-4×1)=4,SO32-中S的价层电子对数=3+
(4-4×1)=4,SO32-中S的价层电子对数=3+![]() (6+2-3×2)=4,所以中心原子均为sp3杂化,故D正确;
(6+2-3×2)=4,所以中心原子均为sp3杂化,故D正确;
故答案为D。

【题目】硫及其化合物对人类的生产和生活有着重要的作用.
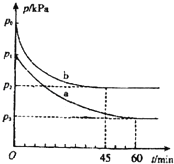
2SO2(g)+O2(g)2SO3(g)△H=﹣198kJmol﹣1是制备硫酸的重要反应.
(1)在容积为V L的密闭容器中起始充入2mol SO2和1mol O2,反应在不同条件下进行,反应体系总压强随时间的变化如图所示.与实验a相比,实验b改变的条件是 ,判断的依据 .
(2)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)SO3(g)+NO(g)△H=﹣42kJmol﹣1.
在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
N(SO2) | N(NO2) | N(NO) | ||
甲 | T1 | 0.80 | 0.20 | 0.18 |
乙 | T2 | 0.20 | 0.80 | 0.16 |
丙 | T3 | 0.20 | 0.30 | a |
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)= ,该温度下的平衡常数 .
②实验丙中,达到平衡时,NO2的转化率为 .
③由表中数据可推知,Tl T2(填“>”“<’’或“=”),判断的理由是 .
【题目】结合元素周期律,结合下列事实推测不合理的是()
事实 | 推测 | |
A | IVA族 | 同族 |
B | HI在230℃时分解,HCl在1500℃时分解 | HF分解温度大于1500℃ |
C | H3PO4是中强酸,H2SO4是强酸 | HClO4是强酸 |
D | Na、Al通常用电解法冶炼 | Mg可用电解法冶炼 |
A.AB.BC.CD.D