题目内容
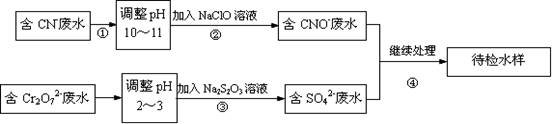
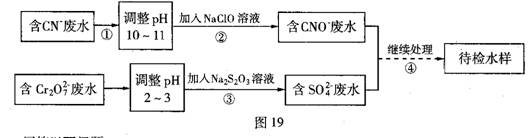
某电镀铜厂有两种废水需要处理,一种废水中含有CN-离子,另一种废水中含有Cr2O72-离子。该厂拟定如图所示的废水处理流程。
回答以下问题:
(1)上述处理废水的流程中主要使用的方法是 。(2分)
(2)②中使用的NaClO溶液呈碱性,用离子方程式解释原因 。(3分)
(3)②中反应后无气体放出,该反应的离子方程式为 。(3分)
(4)③中反应时,每0.4 molCr2O72-转移2.4 mol的电子,该反应的离子方程式为 。(3分)
(5)取少量待检水样于试管中,先加入NaOH溶液,观察到有蓝色沉淀生成,继续加入NaOH溶液,直到不再产生蓝色沉淀为止,再加入Na2S溶液,有黑色沉淀生成,且蓝色沉淀逐渐减少。请你使用化学用语,结合必要的文字解释其原因 。(4分)
(1)氧化还原法
(2)ClO- + H2OHClO+OH- (3)CN-+ ClO- === CNO-+ Cl-
(4)3S2O32- + 4Cr2O72- +26H+ === 6SO42-+ 8Cr3+ + 13H2O (3分)
(5)待检水样中还有Cu2+ Cu2++2OH- ===Cu(OH)2↓
Cu(OH)2(s)+S2-(aq)===CuS(s)+2OH-(aq)(1分,未标状态的不给分,或Cu(OH)2Cu2++2OH-;Cu2++S2-===CuS↓,
CuS比Cu(OH)2更难溶(1分,或溶解度更小)
解析:略

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目

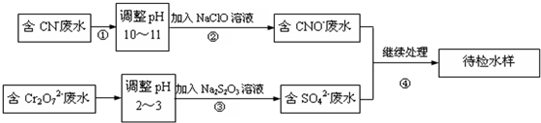
 HClO+OH-
HClO+OH-