题目内容
【题目】(1)pH=2的某酸稀释100倍,pH________4,pH=12的某碱稀释100倍,pH________10。
(2)室温时,将pH=5的H2SO4溶液稀释10倍,c(H+)∶c(SO42-)=________,将稀释后的溶液再稀释100倍,c(H+)∶c(SO42-)=________。
(3)
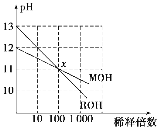
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如上图所示。下列叙述中不正确的是( )
A.MOH是一种弱碱
B.在x点,MOH完全电离
C.在x点,c(M+)=c(R+)
D.稀释前ROH溶液中c(OH-)是MOH溶液中c(OH-)的10倍
【答案】(1)≤ ≥ (2)2∶1 20∶1 (3)B
【解析】(1)若某酸为强酸,则pH=4,若为弱酸,则pH<4;同理,对pH=12的某碱稀释100倍,pH≥10。
(2)pH=5的H2SO4稀释10倍,c(H+)和c(SO42-)同等倍数减小,所以c(H+)∶c(SO42-)=2∶1,若将稀释后的溶液再稀释100倍,其pH≈7,而c(SO42-)=![]() =5×10-9 mol·L-1,所以c(H+)∶c(SO42-)=10-7∶5×10-9=20∶1。
=5×10-9 mol·L-1,所以c(H+)∶c(SO42-)=10-7∶5×10-9=20∶1。
由图知,稀释100倍后ROH的pH变化为2,为强碱,MOH的pH变化为1,为弱碱;x点时ROH与MOH的c(OH-)相等,故c(M+)与c(R+)相等;稀释前ROH的c(OH-)=0.1 mol·L-1,MOH的c(OH-)=0.01 mol·L-1,故D项正确;MOH为弱碱,在任何点都不能完全电离,B项错误。

 导学教程高中新课标系列答案
导学教程高中新课标系列答案【题目】下列叙述不正确的是( )
A | B | C | D |
|
|
|
|
放电闪电时会发生反应:N2+O2═2NO | 利用丁达尔效应证明烧杯中的分散系是胶体 | 蔗糖中加入浓硫酸搅拌后变黑,因为浓硫酸有吸水性 | 加热时熔化的铝不滴落,证明Al2O3的熔点比Al高 |
A.A
B.B
C.C
D.D