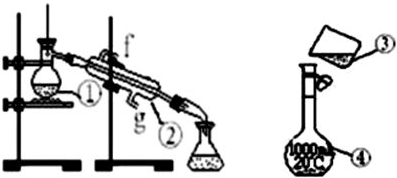
题目内容
3.工业上可由天然气为原料制备甲醇,也可由水煤气合成甲醇.(1)已知2CH4(g)+O2(g)═2CO(g)+4H2(g)△H=akJ/mol;CO(g)+2H2(g)=CH3OH(g)△H=bkJ/mol.试写出由CH4和O2制取甲醇的热化学方程式:2CH4(g)+O2(g)=2CH3OH(g)△H=(a+2b)kJ/mol.
(2)还可以通过下列反应制备甲醇:CO(g)+2H2(g)═CH3OH(g).图甲是反应时CO(g)和CH3OH(g)的浓度随时间t的变化情况.从反应开始到平衡,用CO表示平均反应速率v(CO)=0.075mol•L-1•min-1,该反应的平衡常数表达式为$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$.
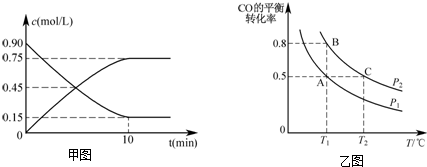
(3)在一容积可变的密闭容器中充入10mol CO和20mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如乙图所示.
①下列说法不能判断该反应达到化学平衡状态的是AC.(填字母)
A.H2的消耗速率等于CH3OH的生成速率的2倍
B.H2的体积分数不再改变
C.体系中H2的转化率和CO的转化率相等
D.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA<PB(填“>、<、=”).
③若达到化学平衡状态A时,容器的体积为20L.如果反应开始时仍充入10molCO和20molH2,则在平衡状态B时容器的体积V(B)=4L.
(4)以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极).
①若KOH溶液足量,则电池负极反应的离子方程式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若电解质溶液中KOH的物质的量为1.0mol,当有0.75mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
分析 (1)已知:①2CH4(g)+O2(g)═2CO(g)+4H2(g)△H=akJ/mol
②CO(g)+2H2(g)=CH3OH(g)△H=bkJ/mol
根据盖斯定律,①+②×2可得:2CH4(g)+O2(g)=2CH3OH(g);
(2)随反应进行,CO浓度减小、甲醇浓度增大,由图可知,10min到达平衡,CO浓度变化为(0.9-0.15)mol/L=0.75mol/L,再根据v=$\frac{△c}{△t}$计算v(CO);
化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
(3)①可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不变化说明到达平衡;
②温度一定时,正反应为气体体积减小的反应,增大压强,平衡向正反应方向移动,CO的转化率增大;
③A、B温度相同,平衡常数相同,若达到化学平衡状态A时,容器的体积为20L,CO转化率为50%,则转化的CO为10mol×50%=5mol,则:
CO(g)+2H2(g)═CH3OH(g)
起始量(mol):10 20 0
变化量(mol):5 10 5
平衡量(mol):5 10 5
平衡常数K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$=$\frac{\frac{5}{20}}{\frac{5}{20}×(\frac{10}{20})^{2}}$=4,
计算B状态时各组分物质的量,再结合平衡常数计算体积;
(4)①原电池负极发生氧化反应,甲醇在负极失去电子,碱性条件下生成碳酸根离子与水;
②当有0.75mol甲醇参与反应时,产生的二氧化碳是0.75mol,和1mol氢氧化钾反应,根据元素守恒:n (K2CO3)+n (KHCO3)=0.75mol,2n (K2CO3)+n(KHCO3)=1mol,联立解得:n (K2CO3)=0.25mol,n (KHCO3)=0.5mol,溶液呈碱性,且水解程度不大.
解答 解:(1)已知:①2CH4(g)+O2(g)═2CO(g)+4H2(g)△H=akJ/mol
②CO(g)+2H2(g)=CH3OH(g)△H=bkJ/mol
根据盖斯定律,①+②×2可得:2CH4(g)+O2(g)=2CH3OH(g)△H=(a+2b)kJ/mol,
故答案为:2CH4(g)+O2(g)=2CH3OH(g)△H=(a+2b)kJ/mol;
(2)随反应进行,CO浓度减小、甲醇浓度增大,由图可知,10min到达平衡,CO浓度变化为(0.9-0.15)mol/L=0.75mol/L,则v(CO)=$\frac{0.75mol/L}{10min}$=0.075mol•L-1•min-1;
CO(g)+2H2(g)═CH3OH(g)的化学平衡常数表达式K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$,
故答案为:0.075mol•L-1•min-1;$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$;
(3)①A.H2的消耗速率等于CH3OH的生成速率的2倍,均表示正反应速率,反应始终按该比例关系进行,不能说明到达平衡,当H2的消耗速率等于CH3OH的消耗速率的2倍时,反应到达平衡,故A错误;
B.H2的体积分数不再改变是化学平衡的特征,达到了平衡,故B正确;
C.氢气、CO的转化率与它们起始物质的量有关,平衡时不一定相等,若起始物质的量之比等于化学计算量之比,转化率始终相等,故C错误;
D.混合气体总质量不变,随反应进行,混合气体总物质的量减小,平均摩尔质量增大,混合气体气体的平均摩尔质量不再改变,说明达到了平衡,故D正确.
故选:AC;
②温度一定时,正反应为气体体积减小的反应,增大压强,平衡向正反应方向移动,CO的转化率增大,故压强PA<PB,
故答案为:<;
③若达到化学平衡状态A时,容器的体积为20L,CO转化率为50%,则转化的CO为10mol×50%=5mol,则:
CO(g)+2H2(g)═CH3OH(g)
起始量(mol):10 20 0
变化量(mol):5 10 5
平衡量(mol):5 10 5
平衡常数K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$=$\frac{\frac{5}{20}}{\frac{5}{20}×(\frac{10}{20})^{2}}$=4,
如果反应开始时仍充入10molCO和20molH2,在平衡状态B时CO转化率为80%,则转化的CO为10mol×80%=8mol,则:
CO(g)+2H2(g)═CH3OH(g)
起始量(mol):10 20 0
变化量(mol):8 16 8
平衡量(mol):2 4 8
设体积为VL,则$\frac{\frac{8}{V}}{\frac{2}{V}×(\frac{4}{V})^{2}}$=4,解得V=4,
故答案为:4;
(4)①原电池负极发生氧化反应,甲醇在负极失去电子,碱性条件下生成碳酸根离子与水,负极电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O,
故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;
②当有0.75mol甲醇参与反应时,产生的二氧化碳是0.75mol,和1mol氢氧化钾反应,根据元素守恒:n (K2CO3)+n (KHCO3)=0.75mol,2n (K2CO3)+n(KHCO3)=1mol,联立解得:n (K2CO3)=0.25mol,n (KHCO3)=0.5mol,溶液呈碱性,溶液中各种离子的物质的量浓度由大到小的顺序是:c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
故答案为:c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
点评 本题考查化学平衡计算、平衡状态判断、盖斯定律应用、原电池、离子浓度大小比较,题目比较综合,需学生具备扎实的基础,是对学生综合能力的考查,(3)中体积计算为难点,注意掌握平衡常数应用,难度中等.

 阅读快车系列答案
阅读快车系列答案| 选项 | 不纯物质(杂质) | 除杂试剂或分离方法 | 必用仪器 |
| A | 碘水 | 四氯化碳 萃取 | 分液漏斗 |
| B | 一氧化碳(二氧化碳) | 澄清石灰水 洗气 | 洗气瓶 |
| C | 硝酸钾(氯化钠) | 直接蒸发结晶 | 蒸发皿 |
| D | 乙醇(水) | 生石灰 蒸馏 | 蒸馏烧瓶 |
| A. | A | B. | B | C. | C | D. | D |
 某研究小组向2L密闭容器中加入一定量的固体A和气体B发生反应:
某研究小组向2L密闭容器中加入一定量的固体A和气体B发生反应:A(s)+2B(g)?D(g)+E(g)△H=Q kJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的物质的量如表:
时间(min) | 0 | 10 | 20 | 30 | 40 | 50 |
| B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
| D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
| E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
(2)30min后,只改变某一条件,反应重新达到平衡,根据表中的数据判断改变的条件可能是ad(填字母编号).
a.通入一定量的B b.加入一定量的固体A
c.升高反应体系温度 d.同时加入0.2molB、0.1molD、0.1molE
(3)维持容器的体积和温度T1不变,当向该容器中加入1.60molB、0.20molD、0.20molE和n molA,达到平衡后,与表格中20分钟时各物质的浓度完全相同时,则投入固体A的物质的量n应不少于0.3mol.
(4)维持容器的体积和温度T1不变,各物质的起始物质的量为:n(A)=1.0mol,n(B)=3.0mol,n(D)=amol,n(E)=0mol,达到平衡后,n(E)=0.50mol,则a=1.5.
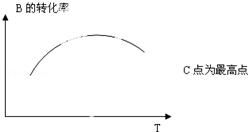
(5)若该密闭容器绝热,实验测得B的转化率B%随温度变化的示意图如图所示.由图可知,Q<0 (填<、>、=),c点v(正)=v(逆)(填<、>、=).
| A. | 32gO2和32gO3所含分子数目都为NA | |
| B. | 标准状况下,11.2 L水中含有的原子数是1.5NA | |
| C. | 0.1mol Fe参与化学反应转移的电子数一定为0.3NA | |
| D. | 标准状况下,5.6L氯气和16.8L氧气混合气体中含有的分子数为NA |
| A. | -1 528.6 kJ•mol-1 | B. | +1 220 kJ•mol-1 | ||
| C. | -1220 kJ•mol-1 | D. | +1 528.6 kJ•mol-1 |
| A. | 每生成16 mol N2转移30 mol电子 | |
| B. | NaN3中N元素被还原 | |
| C. | N2既是氧化剂又是还原剂 | |
| D. | 还原产物与氧化产物质量之比为1:15 |
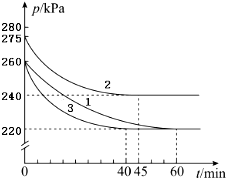 AX(g)+2X2(g)?AX5(g)在容积为10L恒定不变的密闭容器中进行.起始时AX和X2均为1.3mol.分三组进行实验,每组只改变一个条件且改变条件均不同.反应体系总压强随时间的变化如图所示.(计算结果均保留两位有效数字)
AX(g)+2X2(g)?AX5(g)在容积为10L恒定不变的密闭容器中进行.起始时AX和X2均为1.3mol.分三组进行实验,每组只改变一个条件且改变条件均不同.反应体系总压强随时间的变化如图所示.(计算结果均保留两位有效数字)