题目内容
【题目】开放以来,人民生活水平不断提高,更加讲究合理膳食。下列饮食习惯科学的是
A. 多吃肉,少吃蔬菜水果 B. 多饮纯净水,少饮矿泉水
C. 多食用含防腐剂的食品 D. 注饮食的合理搭配
【答案】D
【解析】
A.少吃蔬菜,会造成维生素缺乏,A项错误;
B.纯净水中不含人体所需的微量元素,B项错误;
C.含防腐剂的食物,食用过量会对人体有害,C项错误;
D.注意饮食的合理搭配,合理膳食,有助于人体健康,D项正确;
本题答案选D。

 阅读快车系列答案
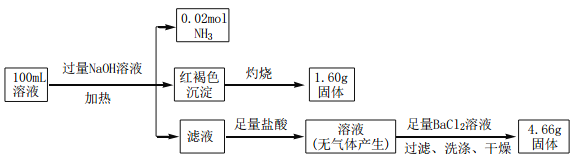
阅读快车系列答案【题目】二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
①CO(g)+2H2(g)![]() CH3OH(g)△H1=-90.7 kJ·mol-1
CH3OH(g)△H1=-90.7 kJ·mol-1
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g)△H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g)△H2=-23.5kJ·mol-1
③CO(g)+H2O(g)![]() CO2(g)+H2(g)△H3=-41.2 kJ·mol-1
CO2(g)+H2(g)△H3=-41.2 kJ·mol-1
回答下列问题:
(1)则反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)的△H=_____________kJ·mol-1。
CH3OCH3(g)+CO2(g)的△H=_____________kJ·mol-1。
(2)在不同温度下按照相同物质的量投料发生反应①,测得CO的平衡转化率与压强的关系如图所示,下列说法正确的是_____________。
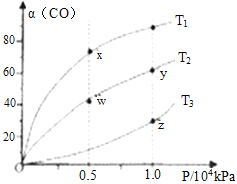
A.反应温度:T1>T2 B.正反应速率:υ正(y)=υ正(w)
C.混合气体密度:ρ(x)>ρ(w) D.混合气体平均摩尔质量:M(y)<M(z)
E.该反应的△S<0、△H<0,所以能在较低温度下自发进行
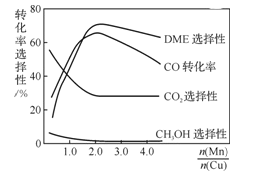
(3)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(DME)。如图回答问题;催化剂中![]() 约为_____________时最有利于二甲醚的合成。
约为_____________时最有利于二甲醚的合成。
(4)高温时二甲醚发生分解反应:CH3OCH3![]() CH4+CO+H2。迅速将二甲醚引入一个504℃的抽成真空的瓶中,在不同时刻t测定瓶内压强P总如下表。
CH4+CO+H2。迅速将二甲醚引入一个504℃的抽成真空的瓶中,在不同时刻t测定瓶内压强P总如下表。
t/min | 0 | 10 | 20 | 30 | 40 | 50 |
P总/kPa | 50.0 | 78.0 | 92.0 | 99.0 | 100 | 100 |
①该反应的平衡常数表达式为Kp=_____________。
②该反应的平衡常数Kp=_____________。(带单位。某一物质的平衡分压=总压×物质的量分数)
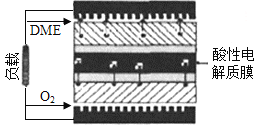
(5)一种以二甲醚作为燃料的燃料电池的工作原理如图所示。则其负极的电极反应式为_______________。该电池的理论输出电压为1.20V,则其能量密度E=_____________(列式计算。能量密度=电池输出电能/燃料质量,1kW·h=3.6×106J,法拉第常数F=96500C·mol-1)。