题目内容
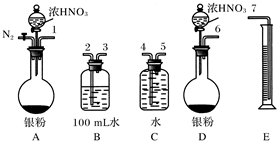
在硝酸生成过程中所排放出来的废气中含有NO和NO2, 它们污染环境。现在氨通过催化还原法将它们转化为无毒气体___________直接排入空气中。写出有关的反应方程式:______________。假设NO和NO2物质的量之比恰好为1:1,则两者的混合物相当于一种酸酐。写出由烧碱溶液吸收这种酸酐的化学方程式_____________。
N2;6NO2
+8NH3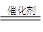 7N2 +12H2O;6NO + 4NH3
7N2 +12H2O;6NO + 4NH3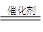 5N2 +6H2O;
5N2 +6H2O;
NO +NO2 + 2NaOH= 2NaNO2 +H2O
【解析】
试题分析:氮的氧化物和氨气之间发生的反应是氮元素之间的氧化还原反应,所以生成的无毒气体是氮气,反应的化学方程式分别是6NO2 +8NH3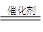 7N2 +12H2O,6NO + 4NH3
7N2 +12H2O,6NO + 4NH3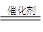 5N2 +6H2O。如果NO和NO2物质的量之比恰好为1:1,则氮元素的平均化合价是
5N2 +6H2O。如果NO和NO2物质的量之比恰好为1:1,则氮元素的平均化合价是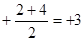 价,所以对应的酸酐是N2O3,相应的钠盐是NaNO3,因此反应的化学方程式是NO+NO2+2NaOH= 2NaNO2+H2O。
价,所以对应的酸酐是N2O3,相应的钠盐是NaNO3,因此反应的化学方程式是NO+NO2+2NaOH= 2NaNO2+H2O。
考点:考查氧化还原反应的有关判断,方程式的书写等
点评:该题的关键是抓住“无毒的气体”,然后根据元素的化合价,即可以准确判断出其产物是氮气,也就是说该反应是氮元素之间发生的氧化还原反应,生成物的价态只能位于中间价态。该题难度不大。

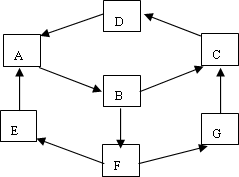
某生利用物质间的互变,设计成一个平面魔方,如下图所示:
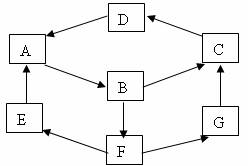
已知①A、B、C、D、G含有同种元素。
②E是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀。
B具有氧化性,能将SO2氧化为F(H2SO4),F与A反应生成E、G。
③
| 纯A(单质) | B溶液 | C固体 | D固体 | G溶液 | |
| 颜色 | 银白色 | 黄色 | 红褐色 | 红棕色 | 浅绿色 |
依据以上信息填空:
(1)请写出E、D的化学式 、 。
(2)请指出A、B、C、D、G所含的同种元素在周期表的位置_________________,该元素原子的电子排布式____________________。
(3)G生成C的过程中所出现的现象为 ,反应式____________________。
(4)写出下列反应的化学方程式:
E→A ; A→B 。
(5)B→F的离子方程式为 。