题目内容
15.2014年8月16日,第二届夏季青年奥林匹克运动会在中国南京开幕.有一种烃分子结构酷似奥林匹克五环旗,科学家称其为奥林匹克烃(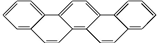 ),是由五个苯环相连形成的.下列有关奥林匹克烃的说法正确的是( )
),是由五个苯环相连形成的.下列有关奥林匹克烃的说法正确的是( )| A. | 该有机物属于芳香族化合物,是苯的同系物 | |
| B. | 能与溴水发生加成反应 | |
| C. | 能使酸性高锰酸钾溶液褪色 | |
| D. | 该烃的分子式为C22H14 |
分析 由结构可知分子式,含5个相连的苯环,为稠环化合物,与苯结构不相似,与溴水、高锰酸钾不反应,以此解答.
解答 解:A.苯的同系物只含一个苯环,故该烃不是苯的同系物,故A错误;
B.分子中不含碳碳双键,故不能与溴水发生加成反应,故B错误;
C.该烃分子中不含碳碳双键,不能使酸性高锰酸钾溶液褪色,故C错误;
D.由结构简式可知有机物分子式为C22H14,故D正确.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重结构对称性、燃烧规律及同分异构体等知识的考查,选项A为解答的易错点,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.现有下列热化学方程式:
①C(s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566kJ•mol-1
③CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H3=-890kJ•mol-1
④CH3CH2OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H4=-1 367kJ•mol-1
下列说法正确的是( )
①C(s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566kJ•mol-1
③CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H3=-890kJ•mol-1
④CH3CH2OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H4=-1 367kJ•mol-1
下列说法正确的是( )
| A. | CO(g)的燃烧热比C(s)的燃烧热大 | |
| B. | △H4>△H3>△H2>△H1 | |
| C. | CO(g)具有的能量比CO2(g)高 | |
| D. | 1 mol C2H5OH蒸气完全燃烧生成CO2和液态水,放出大于1 367 kJ的热量 |
3.合成氨是人类科学技术上的一项重大突破.工业上以天然气为原料合成氨.其生产工艺如下:造气阶段→转化阶段→分离净化→合成阶段
(1)造气阶段的反应为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.1kJ/mol
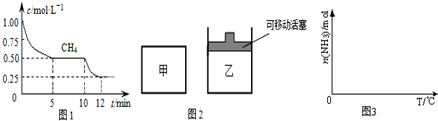
①在一密闭容器中进行上述反应,测得 CH4的物质的量浓度随反应时间的变化如图1所示.反应中处于平衡状态的时间为5min-10min、12min后;10min时,改变的外界条件可能是升高温度.
②如图2所示,在初始容积相等的甲、乙两容器中分别充入等物质的量的CH4和H2O.在相同温度下发生反应,并维持反应过程中温度不变.则达到平衡时,两容器中CH4的转化率大小关系为:α甲(CH4)<α乙(CH4);
(2)转化阶段发生的可逆反应为:CO(g)+H2O(g)?CO2(g)+H2(g),一定温度下,反应的平衡常数为K=1.某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
此时反应中正、逆反应速率的关系式是a(填序号).
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
(3)合成氨反应为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol?1
①依据温度对合成氨反应的影响,在如图3坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图.
②根据勒夏特列原理,简述提高合成氨原料转化率的一种方法增大压强或降低温度或分离液氨.
(1)造气阶段的反应为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.1kJ/mol
①在一密闭容器中进行上述反应,测得 CH4的物质的量浓度随反应时间的变化如图1所示.反应中处于平衡状态的时间为5min-10min、12min后;10min时,改变的外界条件可能是升高温度.
②如图2所示,在初始容积相等的甲、乙两容器中分别充入等物质的量的CH4和H2O.在相同温度下发生反应,并维持反应过程中温度不变.则达到平衡时,两容器中CH4的转化率大小关系为:α甲(CH4)<α乙(CH4);

(2)转化阶段发生的可逆反应为:CO(g)+H2O(g)?CO2(g)+H2(g),一定温度下,反应的平衡常数为K=1.某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
(3)合成氨反应为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol?1
①依据温度对合成氨反应的影响,在如图3坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图.
②根据勒夏特列原理,简述提高合成氨原料转化率的一种方法增大压强或降低温度或分离液氨.
10.将一定量Fe和Fe2O3的混合物放入250mL 2mol/L的硝酸溶液中,反应完全后无固体剩余,生成2.24L NO气体(标准状况),再向反应后的溶液中加入1mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是( )
| A. | 500 mL | B. | 400 mL | C. | 450 mL | D. | 无法确定 |
4.下列说法正确的是( )
| A. | 同种元素的质子数必定相同 | |
| B. | 不同元素原子的质量数必定不同 | |
| C. | 原子核都是由质子和中子构成的 | |
| D. | 凡是核外电子数相同的微粒必定属于同一元素 |
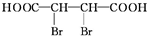 +4NaOH$→_{△}^{醇溶液}$NaOOCC≡CCOONa+2NaBr+4H2O.
+4NaOH$→_{△}^{醇溶液}$NaOOCC≡CCOONa+2NaBr+4H2O. 用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:
用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下: