题目内容
7. 用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:
用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:CuFeS4$→_{800℃}^{O_{2}}$Cu2S$→_{△①}^{O_{2}}$Cu2O$→_{△②}^{Cu_{2}S}$Cu
(1)已知在反应①、②中均生成相同的气体分子,该气体具有漂白性.请分别写出反应①2Cu2S+3O2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+2SO2 .
②的化学方程式是2Cu2O+Cu2S$\frac{\underline{\;\;△\;\;}}{\;}$6Cu+SO2↑、此空删去.
(2)基态铜原子的核外电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1,硫、氧元素相比,第一电离能较大的是氧.
(3)反应①和②生成的气体分子的中心原子的杂化类型是sp2,分子的空间构型是V型.
(4)某学生用硫酸铜溶液与氨水做了一组实验,CuSO4溶液中加氨水生成蓝色沉淀,再加氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4•H2O晶体,请解释加入乙醇后析出晶体的原因乙醇分子极性比水分子极性弱,加入乙醇降低溶剂的极性,从而降低溶质的溶解度;在该晶体中存在化学键的种类有共价键、离子键、配位键.
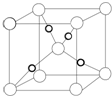
(5)Cu2O的晶胞结构如图所示,该晶胞的边长为a cm,则Cu2O的密度为$\frac{320}{{a}^{3}×{N}_{A}}$g•cm-3(用NA表示阿伏加德罗常数的数值).
分析 (1)由题给信息知反应①是Cu2S和O2反应生成Cu2O的反应,由于Cu元素的化合价不变,O元素的化合价降低,则S元素的化合价一定升高,结合所学知识知道生成的物质为二氧化硫.化学方程式为同理,反应②是Cu2O和Cu2S反应生成Cu的反应,Cu元素的化合价降低,元素S的化合价升高生成二氧化硫,知道了反应物和生成物,配平化学方程式即可;
(2)Cu是29号元素,原子核外电子数为29,根据核外电子排布规律书写铜的基态原子价电子排布式;
同主族元素第一电离能自上而下逐渐减小;
(3)由(1)分析知反应①②生成的相同气体分子是SO2,SO2中价层电子对个数=2$\frac{1}{2}$(6-2×2)=3,且含有一个孤电子对,所以其空间构型是V型,S原子采用sp2杂化;
(4)根据相似相容原理判断;阴阳离子存在离子键,非金属元素间易形成共价键,配合物中存在配位键;
(5)由均摊法计算氧化亚铜晶胞中Cu原子和O原子的数目,根据密度计算公式ρ=$\frac{m}{V}$计算即可.
解答 解:(1)由题给信息知反应①是Cu2S和O2反应生成Cu2O的反应,由于Cu元素的化合价不变,O元素的化合价降低,则S元素的化合价一定升高,结合所学知识知道生成的物质为二氧化硫.化学方程式为2Cu2S+3O2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+2SO2 ;
反应②是Cu2O和Cu2S反应生成Cu的反应,Cu元素的化合价降低,元素S的化合价升高生成二氧化硫,化学方程式为2Cu2O+Cu2S$\frac{\underline{\;\;△\;\;}}{\;}$6Cu+SO2↑;
故答案为:2Cu2S+3O2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+2SO2 ;2Cu2O+Cu2S$\frac{\underline{\;\;△\;\;}}{\;}$6Cu+SO2↑;
(2)Cu是29号元素,原子核外电子数为29,铜的基态原子核外电子排布式1s22s22p63s23p63d104s1或[Ar]3d104s1,同主族元素第一电离能自上而下逐渐减小,所以第一电离能较大的是氧;
故答案为:1s22s22p63s23p63d104s1或[Ar]3d104s1;氧;
(3)由(1)分析知反应①②生成的相同气体分子是SO2,SO2中价层电子对个数=2+$\frac{1}{2}$(6-2×2)=3,所以S原子采用sp2杂化,由于含有一个孤电子对,其空间构型是V型;
故答案为:sp2;V型;
(4)在水中得到深蓝色透明溶液,加入乙醇析出晶体,说明在乙醇中溶解性降低,根据相似相溶分析:乙醇分子极性弱于水的极性,在乙醇中溶解度降低;[Cu(NH3)4]SO4中硫酸根离子和[Cu(NH3)4]2+存在离子键,N原子和铜原子之间存在配位键,NH3中H和N之间存在共价键,所以[Cu(NH3)4]SO4中所含的化学键有共价键、离子键、配位键;
故答案为:乙醇分子极性比水分子极性弱,加入乙醇降低溶剂的极性,从而降低溶质的溶解度;共价键、离子键、配位键;
(5)O原子在晶胞的顶点和体心,故O原子数=8×$\frac{1}{8}$+1=2,Cu原子全部在体心,故Cu原子数=4,即一个氧化亚铜晶胞中有2个O原子和4个Cu原子,则该氧化物的密度ρ=$\frac{m}{V}$=$\frac{\frac{64g/mol×4+32g/mol×2}{{N}_{A}}}{{a}^{3}}$g•cm-3=$\frac{320}{{a}^{3}×{N}_{A}}$g•cm-3.
故答案为:$\frac{320}{{a}^{3}×{N}_{A}}$.
点评 本题考查较为全面,涉及到化学方程式的书写、电子排布式、分子空间构型、杂化类型的判断以及有关晶体的计算,但解题具有较强的方法性和规律性,学习中注意总结如何书写电子排布式,如何判断分子空间构型以及有关晶体计算等方法,题目难度中等.

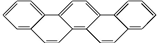 ),是由五个苯环相连形成的.下列有关奥林匹克烃的说法正确的是( )
),是由五个苯环相连形成的.下列有关奥林匹克烃的说法正确的是( )| A. | 该有机物属于芳香族化合物,是苯的同系物 | |
| B. | 能与溴水发生加成反应 | |
| C. | 能使酸性高锰酸钾溶液褪色 | |
| D. | 该烃的分子式为C22H14 |
| 序号 | 实验内容 | 实验目的 |
| A | 在滴有酚酞的Na2CO3溶液中,滴加入BaC12溶液,溶液红色逐渐褪去 | 证明Na2CO3溶液中存在水解平衡 |
| B | 将Al泊插入浓硝酸中,无现象 | 证明Al和浓硝酸不反应 |
| C | 将两个完全相同且充满NO2的密闭烧瓶,分别浸泡于热水、冰水中 | 探究温度对化学平衡状态的影响 |
| D | 向同体积同浓度的H2O2溶液中,分别加入1mL同浓度的CuSO4、FeCl3溶液 | 比较Cu2+、Fe3+对H2O2分解速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 2NO2?N2O4-①N2O4?2NO2-②,反应①的化学平衡常数是反应②的倒数 | |
| B. | 已知H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,将100.0mL 0.05mol/LBa(OH)2溶液与100.0mL 0.05mol/L H2SO4溶液混合,在298K、101kPa条件下放出热量为0.573kJ | |
| C. | 已知298K 时,0.10mol/L HAc的电离度为1.32%.在0.10mol/L HAc 和0.10mol/LNaAc的混合溶液20.00mL中,有如下变化:HAc?H++Ac----①,NaAc=Na++Ac-----②,Ac-+H2O?HAc+OH-----③,向该溶液中滴入几滴稀盐酸,溶液的pH保持相对稳定 | |
| D. | 将明矾与纯碱溶液混合,有沉淀产生,该沉淀的成分为碳酸铝 |
| A. | 无色溶液中:Na+、Cu2+、Cl-、NO3- | |
| B. | 强酸性溶液中:Na+、K+、OH-、SiO32- | |
| C. | 能与Al反应放出氢气的溶液中:K+、NH4+、HCO3-、Cl- | |
| D. | 澄清透明溶液中:Fe2+、Na+、SO42-、Cl- |
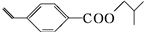 )是一种化工原料,其合成路线如下:
)是一种化工原料,其合成路线如下:
 (填结构简式).
(填结构简式). ;锂暴露在湿空气中时,会迅速地失去金属光泽、表面开始变黑,更长时间则变成白色.生成的化合物是氮化锂、氢氧化锂,最终生成碳酸锂.写出生成氮化锂的化学方程式6Li+N2=2Li3N.锂在空气中燃烧,发出浅蓝色的火焰,放出浓厚的白烟,生成相应氧化物Li2O(填化学式).
;锂暴露在湿空气中时,会迅速地失去金属光泽、表面开始变黑,更长时间则变成白色.生成的化合物是氮化锂、氢氧化锂,最终生成碳酸锂.写出生成氮化锂的化学方程式6Li+N2=2Li3N.锂在空气中燃烧,发出浅蓝色的火焰,放出浓厚的白烟,生成相应氧化物Li2O(填化学式).