题目内容
【题目】碳及其化合物在生产、生活中有广泛的应用,按要求回答问题:
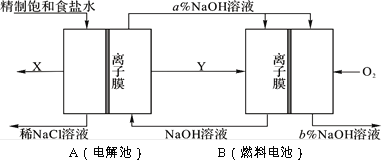
(1)CO2可通过反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)转化成有机物实现碳循环。一定条件下,在体积为1 L的密闭容器中,充入 1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g)转化成有机物实现碳循环。一定条件下,在体积为1 L的密闭容器中,充入 1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
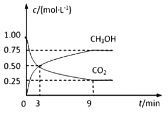
从3 min到9 min内,v(H2)=_____mol·L1·min1。平衡时H2的转化率为________。平衡时混合气体中CO2(g)的体积分数是________。一定温度下,第9分钟时v逆(CH3OH) _______第3分钟时v正(CH3OH)(填“大于”、“小于”或“等于”)。
(2)如图,将锌片、C棒通过导线相连,置于稀硫酸中。
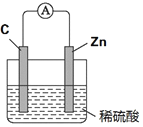
该装置工作时,溶液中的SO42-向____极(填“C”或“Zn”)移动;电子沿导线流入_______极(填“C”或“Zn”)。写出正极的电极反应式____。若正极产生11.2L气体(标况下),则电路中应该有___mol电子发生了转移。
【答案】0.125 75﹪ 10﹪ 小于 Zn C 2H++2e-=H2↑ 1
【解析】
此题为化学反应原理的综合题,主要考察简单的化学反应速率和平衡、三段式的计算以及原电池的相关内容。
(1)从3 min到9 min内,![]() ;平衡时氢气的转化率和平衡时混合气体中CO2的体积分数可用三段式进行计算,
;平衡时氢气的转化率和平衡时混合气体中CO2的体积分数可用三段式进行计算,
CO2(g) | + | 3H2(g) |
| CH3OH(g) | + | H2O(g) | |
c0 | 1 | 3 | 0 | 0 | |||
Δc | 0.75 | 2.25 | 0.75 | 0.75 | |||
c | 0.25 | 0.75 | 0.75 | 0.75 |
所以平衡时氢气的转化率=2.25÷3×100%=75%;
混合气体中CO2的体积分数=0.25÷(0.25+0.75+0.75+0.75)×100%=10%;
第9分钟时反应达到平衡,则v逆(CH3OH) <第3分钟时v正(CH3OH);
(2)此原电池锌片作负极,C棒作正极材料,氢离子在正极的电子生成氢气;
该装置工作时,溶液中的SO42-向负极Zn移动,电子沿导线流入正极C;
正极的电极反应为2H++2e-=H2↑;
若正极产生11.2L气体(标况下),则气体的物质的量为0.5mol,则电路中应该有1mol电子发生了转移。

【题目】温度为T0C时,向2.0L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A. 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0
B. 反应在前50 s的平均速率为v(PCl3)=0.0032mol·L-1·s-1
C. 相同温度下,起始时向容器中充入2.0mol PCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
D. 相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20molCl2,达到平衡时,c(PCl5) > 0.4mol·L-1