题目内容
【题目】玻璃是一种重要的传统无机非金属材料。
(1)普通玻璃又称为钠玻璃,试写出生产普通玻璃过程中发生反应的化学方程式:_____________,_______________。
(2)实验室用于盛放碱性试剂的试剂瓶不用磨口玻璃塞的原因是(用离子方程式表示):______________;玻璃试剂瓶不能盛放氢氟酸的原因是(用化学方程式表示):______________。
(3)有一种特殊玻璃为钾玻璃,其热膨胀系数较小,较难熔化,较难受化学药品的侵蚀,可用于制作一般的化学仪器。现以石英砂、苛性钾、熟石灰为原料,熔制钾玻璃,质量比为75:28:37(假定这些原料不含杂质),试用氧化物的形式表示该钾玻璃的组成________。
【答案】CaCO3+SiO2![]() CaSiO3+CO2↑ Na2CO3+SiO2
CaSiO3+CO2↑ Na2CO3+SiO2 ![]() Na2SiO3+CO2↑ 2OH-+SiO2=SiO32-+H2O SiO2+4HF=SiF4↑+2H2O K2O2CaO5SiO2
Na2SiO3+CO2↑ 2OH-+SiO2=SiO32-+H2O SiO2+4HF=SiF4↑+2H2O K2O2CaO5SiO2
【解析】
(1)工业上制取玻璃的原料有石英、纯碱和石灰石。在高温下,在玻璃熔炉中石灰石与石英反应产生硅酸钙和二氧化碳;纯碱与石英反应产生硅酸钠和二氧化碳;
(2)玻璃中含有的SiO2与强碱反应产生硅酸盐和水,硅酸钠具有粘性,将试剂瓶与玻璃塞黏在一起;SiO2与氢氟酸反应产生SiF4和水;
(3)利用质量分数确定个数比,用氧化物表示玻璃的组成为活泼金属氧化物、较活泼金属氧化物、二氧化硅、水的顺序书写。
(1)在高温下,在玻璃熔炉中石灰石与石英反应产生硅酸钙和二氧化碳,纯碱与石英反应产生硅酸钠和二氧化碳,反应方程式为:CaCO3+SiO2 ![]() CaSiO3+CO2↑,Na2CO3+SiO2
CaSiO3+CO2↑,Na2CO3+SiO2![]() Na2SiO3+CO2↑;
Na2SiO3+CO2↑;
(2)玻璃的成分中含有SiO2与碱性物质NaOH反应,产生具有粘性的硅酸钠,将试剂瓶与玻璃塞黏在一起,反应的离子方程式为:SiO2+2OH-=SiO32-+H2O;玻璃中含有SiO2,能够与氢氟酸反应产生SiF4和水,反应方程式为:SiO2+4HF=SiF4↑+2H2O;
(3)由石英砂、苛性钾、熟石灰质量比为75:28:37,根据元素原子守恒,n(K2O):n(CaO):n(SiO2)=![]() n(KOH):n[Ca(OH)2]:n(SiO2)=
n(KOH):n[Ca(OH)2]:n(SiO2)= ![]() :
:![]() :
:![]() =1:2:5,用氧化物形式表示玻璃的组成时的书写顺序为:活泼金属氧化物较活泼金属氧化物二氧化硅水的顺序,则玻璃为K2O2CaO5SiO2。
=1:2:5,用氧化物形式表示玻璃的组成时的书写顺序为:活泼金属氧化物较活泼金属氧化物二氧化硅水的顺序,则玻璃为K2O2CaO5SiO2。

 名校课堂系列答案
名校课堂系列答案【题目】如图装置可用于收集气体并验证其某些化学性质能达到目的是
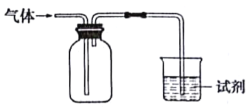
选项 | 气体 | 试剂 | 现象 | 结论 |
A | NH3 | 酚酞试液 | 溶液变红色 | 氨水显碱性 |
B | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性和漂白性 |
C | C2H4 | 溴水 | 溶液褪色 | C2H4分子中含碳碳双键 |
D | X | KI淀粉溶液 | 溶液变蓝 | X可能是NO2 |
A.AB.BC.CD.D