题目内容
对于常温下pH=1的硝酸溶液,有关叙述:
①该溶液1 mL稀释至100 mL后, pH="3"
②向该溶液中加入等体积、pH=13的氢氧化钡溶液恰好完全中和
③该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为
④向该溶液中加入等体积、等浓度的氨水,所得溶液pH=7
其中正确的是
①该溶液1 mL稀释至100 mL后, pH="3"
②向该溶液中加入等体积、pH=13的氢氧化钡溶液恰好完全中和
③该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为

④向该溶液中加入等体积、等浓度的氨水,所得溶液pH=7
其中正确的是
| A.①② | B.①③ | C.②④ | D.③④ |
A
试题分析:硝酸是强酸,稀释100倍后溶液的pH增大2个单位,①正确;硝酸和氢氧化钡都是强酸和强碱,且溶液中氢离子和OH-浓度都是相等的,二者恰好反应,溶液显中性,②正确;溶液中水电离出的c(H+)就等于溶液中OH-浓度,所以根据水的离子积常数可知,该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为
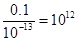 ,③不正确;④不正确,此时二者恰好反应,但生成的氯化铵水解,溶液显酸性,答案选A。
,③不正确;④不正确,此时二者恰好反应,但生成的氯化铵水解,溶液显酸性,答案选A。点评:在判断中和反应后溶液的酸碱性时,应该首先判断酸或碱的过量问题。只有当酸或碱恰好反应时,才能考虑生成的盐是否水解。

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
 Cu2++2OH-,Ksp=c(Cu2+)·c2(OH-)=2×10-20。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。
Cu2++2OH-,Ksp=c(Cu2+)·c2(OH-)=2×10-20。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。