题目内容
12.工业生产硝酸铵的流程图如图.请回答: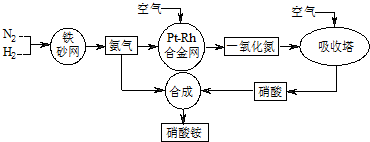
(1)已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.
①在500℃、2.02×107Pa和铁催化条件下向一密闭容器中充入1molN2和3molH2,充分反应后,放出的热量<(填“<”、“>”或“=”)92.4kJ,理由是该反应为可逆反应.
②为提高氨的产量,获得更大的效益,实际生产中宜采取的措施有BCEF.
A.降低温度 B.最适合催化剂活性的适当高温 C.增大压强
D.降低压强 E.循环利用和不断补充氮气 F.及时移出氨
(2)已知铂铑合金网未预热也会发热.写出氨催化氧化的化学方程式:4NH3+5O2$\frac{\underline{\;加热\;}}{\;}$4NO+6H2O,该反应的化学平衡常数表达式K=$\frac{{c}^{4}(NO){c}^{6}(H{\;}_{2}O)}{{c}^{4}(N{H}_{3}){c}^{5}({O}_{2})}$,当温度升高时,K值减小(填“增大”、“减小”或“不变”).
(3)在一定温度和压强的密闭容器中,将平均相对分子质量为8.5的H2和N2混合,当该反应达到平衡时,测出平衡混合气的平均相对分子质量为10,请计算此时H2的转化率(写出计算过程).
分析 (1)①热反应方程式中反应热是指完全反全放出的热量,而合成氨反应是可逆反应,放出的热量比完全反应少;
②该反应是气体体积减小的放热反应,根据影响平衡移动和化学反应速率的因素判断,为提高氨的产量,获得更大的效益,既要考滤反应物质的转化率,又要考滤反应速率,据此答题;
(2)氨具胡还原性,被氧化成一氧化氮和水;化学平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积;
(3)根据平均式量利用十字交叉法求出两者的物质的量之比,然后根据平均式量为10利用平衡三部曲求出各自的物质的量,最终求出转化率.
解答 解:(1)①因为可逆反应不可能完全进行到底,放出的热量比完全反应少,
故答案为:<,该反应为可逆反应;
②因增大反应物的浓度,减少生成物的浓度,增大压强,降低温度工业合成氨反应向正反应方向移动,氢气的转化率提高,但在实际生产中不能用低温,因为温度低化学反应速率慢,最适合催化剂活性的适当高温,保持较好的反应速率,
故答案为:BCEF;
(2)因为NH3具有还原性,能被氧气氧化:4NH3+5O2$\frac{\underline{\;加热\;}}{\;}$4NO+6H2O,该反应的平衡常数K=$\frac{{c}^{4}(NO){c}^{6}(H{\;}_{2}O)}{{c}^{4}(N{H}_{3}){c}^{5}({O}_{2})}$,因工业合成氨反应是放热反应,升高温度,平衡向逆反应方向移动,化学平衡常数减小,
故答案为:4NH3+5O2$\frac{\underline{\;加热\;}}{\;}$4NO+6H2O,$\frac{{c}^{4}(NO){c}^{6}(H{\;}_{2}O)}{{c}^{4}(N{H}_{3}){c}^{5}({O}_{2})}$,减小;
(3)十字交叉法:平均相对分子质量为8.5的H2和N2物质的量比=(28-8.5):(8.5-2)=3:1
平衡三部曲:N2 +3H2 ?2NH3
起始 1 3 0
转化 x 3x 2x
平衡 1-x 3-3x 2x
平衡混合气的平均相对分子质量为10,对应的相对分子质量:$\frac{28×1+2×3}{(1-x)+(3-3x)+2x}$=10,x=0.3,则H2转化率为$\frac{3×0.3}{3}$×100%=30%,
故答案为:30%.
点评 本题结合工业生产硝酸铵的流程图考查了可逆反应、化学平衡常数、十字交叉法等,试题的综合性较强,学生做起来有一定的难度.

 习题精选系列答案
习题精选系列答案| A. | 75 mL 2 mol•L-1 的NH4Cl | B. | 150 mL 1 mol•L-1 的NaCl | ||
| C. | 50 mL 1.5 mol•L-1 的CaCl2 | D. | 50 mL 3 mol•L-1 的KClO3 |
(1)C的生成速率与A的分解速率相等; (2)单位时间生成2mol A,同时消耗3mol B;
(3)A、B、C的分子数目比为1:3:2. (4)A、B、C各物质的物质的量不再变化;
(5)混合气体的总压强不再变化; (6)混合气体的物质的量不再变化.
| A. | (1)(2) | B. | (2)(4) | C. | (2)(5) | D. | (3)(6) |
| A. | 4:5:2 | B. | 4:6:2 | C. | 6:4:3 | D. | 6:2:3 |
| A. | 2H2O(l)═2H2(g)+O2(g)△H=+571.6 kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=+571.6 kJ•mol-1 | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ•mol-1 |

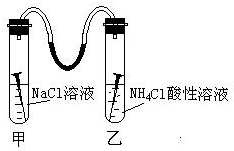 如图所示,甲、乙两试管中各放一枚铁钉,用装有少量水的玻璃弯管连接,甲试管中是NaCl溶液,乙试管中是NH4Cl溶液(显酸性),数天后,观察到的现象是:玻璃弯管液面左高右低(填高、低)请写出甲试管中正极反应式:O2+2H2O+4e-═4OH-.乙试管负极反应式
如图所示,甲、乙两试管中各放一枚铁钉,用装有少量水的玻璃弯管连接,甲试管中是NaCl溶液,乙试管中是NH4Cl溶液(显酸性),数天后,观察到的现象是:玻璃弯管液面左高右低(填高、低)请写出甲试管中正极反应式:O2+2H2O+4e-═4OH-.乙试管负极反应式