��Ŀ����
����Ŀ��A�������ɲ�Ҷ��һ���л����ܱ��������֪��
��A������ԭ�Ӻ˴Ź�������6�֡�
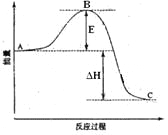
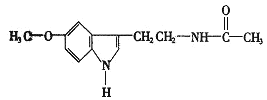
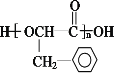
��H�ṹ��ʽΪ��
���ǵĹ�ϵ���£�

��ش��������⣺
(1)�л���X�Ľṹ��ʽΪ_______
(2)ָ����Ӧ�١��ڡ��۵ķ�Ӧ���ͣ���______�� ______��______��
(3)д�����з�Ӧ�Ļ�ѧ����ʽ(�л���д�ṹ��ʽ)
��D��E��_____________
��F��Ũ������������·������۷�Ӧ�Ļ�ѧ����ʽ��____________
(4)д�����з�������������A��ͬ���칹��Ľṹ��ʽ��__________
�ٱ�����ֻ��һ��ȡ����
���ܷ���ˮ�ⷴӦ
������������Һ������Ӧ
���𰸡�![]() ȡ����Ӧ �ӳɷ�Ӧ ������Ӧ
ȡ����Ӧ �ӳɷ�Ӧ ������Ӧ ![]() +2NaOH
+2NaOH![]()
![]() +NaCl+H2O n
+NaCl+H2O n![]()
![]()
 +��n-1��H2O
+��n-1��H2O ![]() ��
��![]()
��������
F��Ũ���ᡢ��������������H�����H�Ľṹ��֪FΪ![]() ��A������̼�����Ʒ�Ӧ����C����A�к���-COOH��A��HCl�����ӳɷ�Ӧ����D��D����ˮ�ⷴӦ����E��E�ữ�õ�F����EΪ
��A������̼�����Ʒ�Ӧ����C����A�к���-COOH��A��HCl�����ӳɷ�Ӧ����D��D����ˮ�ⷴӦ����E��E�ữ�õ�F����EΪ![]() ��DΪ
��DΪ![]() ��AΪ
��AΪ![]() ��CΪ
��CΪ![]() ��B����Cu����������������������G����BΪCH3CH2OH��GΪCH3CHO����XΪ
��B����Cu����������������������G����BΪCH3CH2OH��GΪCH3CHO����XΪ![]() ���ݴ˽��
���ݴ˽��
F��Ũ���ᡢ��������������H�����H�Ľṹ��֪FΪ![]() ��A������̼�����Ʒ�Ӧ����C����A�к���-COOH��A��HCl�����ӳɷ�Ӧ����D��D����ˮ�ⷴӦ����E��E�ữ�õ�F����EΪ
��A������̼�����Ʒ�Ӧ����C����A�к���-COOH��A��HCl�����ӳɷ�Ӧ����D��D����ˮ�ⷴӦ����E��E�ữ�õ�F����EΪ![]() ��DΪ
��DΪ![]() ��AΪ
��AΪ![]() ��CΪ
��CΪ![]() ��B����Cu����������������������G����BΪCH3CH2OH��GΪCH3CHO����XΪ
��B����Cu����������������������G����BΪCH3CH2OH��GΪCH3CHO����XΪ![]() ��
��
��1��������������֪���л���X�Ľṹ��ʽΪ![]() ��
��
��2����Ӧ��ȡ����Ӧ����Ӧ�����ڼӳɷ�Ӧ����Ӧ������������Ӧ��
��3��D-E�Ļ�ѧ��Ӧ����ʽΪ��![]() +2NaOH
+2NaOH![]()
![]() +NaCl+H2O��
+NaCl+H2O��
F��Ũ������������·������۷�Ӧ�Ļ�ѧ����ʽ��n![]()
![]()
 +��n-1��H2O��
+��n-1��H2O��
��4����������������A��![]() ����ͬ���칹�壺�ٱ�����ֻ��һ��ȡ���� ���ܷ���ˮ�ⷴӦ��������������Һ������Ӧ��Ӧ���м����γɵ�����������������ͬ���칹���У�
����ͬ���칹�壺�ٱ�����ֻ��һ��ȡ���� ���ܷ���ˮ�ⷴӦ��������������Һ������Ӧ��Ӧ���м����γɵ�����������������ͬ���칹���У�![]() ��
��![]() ��
��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�