题目内容
某温度时,在2L密闭容器中气态物质CO和H2反应生成气态物质Z,它们的物质的量随时间的变化如下表所示.
(1)根据上表中数据,在图中画出CO、Z的物质的量的浓度(c)随时间(t)变化的曲线:
(2)体系中发生反应的化学方程式是______.
(3)在3-5min时间内产物Z的平均反应速率:______.
| t/min | CO/mol | H2/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.10 |
| 3 | 0.75 | 0.50 | 0.25 |
| 5 | 0.65 | 0.30 | 0.35 |
| 7 | 0.55 | 0.10 | 0.45 |
| 9 | 0.55 | 0.10 | 0.45 |
| 10 | 0.55 | 0.10 | 0.45 |
(2)体系中发生反应的化学方程式是______.
(3)在3-5min时间内产物Z的平均反应速率:______.

(1)由表中数据可知,开始CO的物质的量为1mol,故CO的起始浓度为
=0.5mol/L,Z的起始浓度为0,7min时反应到达平衡,平衡时CO的物质的量为0.55mol,故CO的平衡浓度为
=0.275mol/L,平衡时Z的物质的量为0.45mol,故Z的平衡浓度为
=0.225mol/L,故CO、Z的物质的量的浓度(c)随时间(t)变化的曲线为:
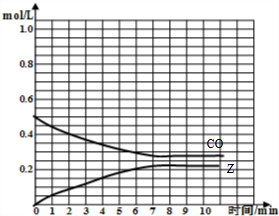 ,
,
故答案为: ;
;
(2)由表中数据可知,7min时反应到达平衡,平衡时CO的物质的量为0.55mol,故△n(CO)=1mol-0.55mol=0.45mol,H2的物质的量为0.1mol,故n(H2)=1mol-0.1mol=0.9mol,平衡时Z的物质的量为0.45mol,故CO、H2、Z的化学计量数之比为0.45mol:0.9mol:0.45mol=1:2:1,即CO+2H2=Z,故Z的分子式为CH4O,结构式为CH3OH,故该反应为CO+2H2?CH3OH,
故答案为:CO+2H2?CH3OH;
(3)由表中数据可知3-5min时间内产物Z的物质的量变化量为0.35mol-0.25mol=0.1mol,
故v(Z)=
=0.025mol/(L?min),
故答案为:0.025mol/(L?min).
| 1mol |
| 2L |
| 0.55mol |
| 2L |
| 0.45mol |
| 2L |
 ,
,故答案为:
 ;
;(2)由表中数据可知,7min时反应到达平衡,平衡时CO的物质的量为0.55mol,故△n(CO)=1mol-0.55mol=0.45mol,H2的物质的量为0.1mol,故n(H2)=1mol-0.1mol=0.9mol,平衡时Z的物质的量为0.45mol,故CO、H2、Z的化学计量数之比为0.45mol:0.9mol:0.45mol=1:2:1,即CO+2H2=Z,故Z的分子式为CH4O,结构式为CH3OH,故该反应为CO+2H2?CH3OH,
故答案为:CO+2H2?CH3OH;
(3)由表中数据可知3-5min时间内产物Z的物质的量变化量为0.35mol-0.25mol=0.1mol,
故v(Z)=
| ||
| 5min-3min |
故答案为:0.025mol/(L?min).

练习册系列答案
相关题目



 pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).
pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).