题目内容
【题目】雾霾天气严重影响人们的生活,汽车尾气所排放的氮氧化物及燃煤所排放的硫氧化物是造成雾霾的重要原因。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:
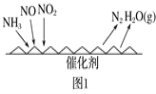
①由图1可知,SCR技术中的氧化剂为___。已知c(NO2)∶c(NO)=1∶4时脱氮效果最佳,此时对应的脱氮反应的化学方程式为__。
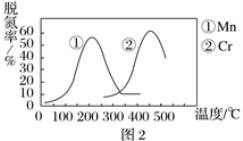
②图2是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳的催化剂和相应的温度分别为___。
(2)改善能源结构是治理雾霾问题的最直接有效途径。二甲醚是一种清洁能源,可用合成气在催化剂下制备二甲醚,其反应为:2CO(g)+4H2(g)![]() CH3OCH3 (g)+H2O(g) ΔH。
CH3OCH3 (g)+H2O(g) ΔH。
已知在一定条件下,该反应中CO的平衡转化率α随温度、投料比![]() 的变化曲线如图3所示。
的变化曲线如图3所示。
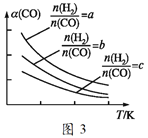
①a、b、c按由大到小的顺序排序为_______;ΔH_______0(填“>”“<”或“=”)。
②对于气相反应,用某组分(B)的平衡分压p(B)代替物质的量浓度c(B)也可以表示平衡常数(记作Kp),则该反应平衡常数的表达式Kp=__。
③在恒容密闭容器里按体积比为1∶2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列能说明平衡一定向逆反应方向移动的是______。
A.一氧化碳的转化率减小
B.容器的压强增大
C.化学平衡常数K值减小
D.逆反应速率先增大后减小
E.混合气体的密度增大
【答案】NO、NO2 NH3+8NO+2NO2===9N2+12H2O Mn、200℃左右 a>b>c < ![]() CD
CD
【解析】
(1)
①由图中得失电子可知,氮氧化物中的氮元素价态降低,故NO、NO2是氧化剂。根据c(NO2)∶c(NO)=1∶4得出方程式为NH3+8NO+2NO2===9N2+12H2O;
②条件越低,效果越好,根据图中可知,温度越低,脱氮效率越高,是最优选择,所以对应催化剂为Mn、温度为200℃左右;
(2)
①根据图像可知,增大氢气的浓度,平衡右移,一氧化碳的转化率增大,所以a>b>c;温度升高,转化率降低,说明该反应为放热反应,ΔH<0;
②根据化学反应平衡常数的计算方法,将所有的物质的量浓度换成压强即可,所以常数为![]() ;
;
③A.增加CO气体的浓度,平衡右移,一氧化碳的转化率减小,A项错误;
B.如果容器的容积和温度不变,充入和反应无关的气体,容器的压强增大,各物质的浓度不变,平衡不移动,B项错误;
C.该反应为放热反应,升高温度,平衡左移,化学平衡常数K值减小,C项正确;
D.逆反应速率先增大后减小,说明逆反应速率大于正反应速率,平衡左移,D项正确;
E.该反应在反应前后混合气体的质量不发生变化,混合气体的密度增大,说明气体的体积减小,相当于增大压强,平衡右移,E项错误;
答案选CD。

 名校通行证有效作业系列答案
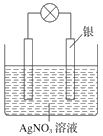
名校通行证有效作业系列答案【题目】向如图装置中缓慢地通入气体X,若关闭活塞,则品红溶液无变化,而澄清石灰水变浑浊;若打开活塞,则品红溶液褪色,加热后又恢复红色.据此判断气体X和洗气瓶内溶液Y分别可能是 ( )
A | B | C | D | |
X | SO2 | H2S | CO2 | Cl2 |
Y | 饱和NaHCO3 | 浓硫酸 | Na2SO3 | NaHCO3 |

A.A正确B.B正确C.C正确D.D正确
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 反应前2 min的平均速率v(Z)=2.0×10-3 mol·(L·min)-1
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大