题目内容
【题目】某可逆反应:2A(g)![]() B(g)+D(g)在密闭固定容积的容器中4种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
B(g)+D(g)在密闭固定容积的容器中4种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
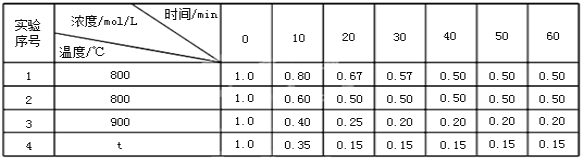
(1)实验1中,在10~20min内,以物质A表示的平均反应速率为_____。
(2)0~20min内,实验2比实验1的反应速率(“快”或“慢”)_____,其原因可能是_____。
(3)实验3比实验1的反应速率(填“快”或“慢”)_____,其原因可能是_____。
(4)从表中可以看出,t_____900(填“>”、“<”、“=”)。
(5)实验3中40分钟时υ(正)_____υ(逆)(填“>”、“<”、“=”)。
(6)实验4中50分钟时B的浓度为_____。
【答案】0.013mol·L-1·min-1 快 实验2使用了催化剂 快 实验3比实验1的温度高 > = 0.425mol/L
【解析】
(1)根据速率公式υ(A)=![]() =(0.8-0.67) mol·L-1÷10min= 0.013 mol·L-1·min-1 ,因此,本题正确答案是0.013mol·L-1·min-1 ;
=(0.8-0.67) mol·L-1÷10min= 0.013 mol·L-1·min-1 ,因此,本题正确答案是0.013mol·L-1·min-1 ;
(2)实验1、2起始量相同,温度相同,平衡浓度相同,但实验2达到平衡所需要的时间短,反应速率快,说明加入了催化剂,加快反应速率,平衡不变,因此,正确答案是:快;使用了催化剂;
(3)实验1、3起始量相同,但实验3达到平衡所需要的时间短,反应速率快,根据图表可以知道,实验3温度比实验1高,因此,答案是:快;实验3的温度比实验1高;
(4)从表中可以看出,实验4比实验3达到平衡所需时间更短,反应程度更大,说明温度比实验3更高,即t>900。答案:>。
(5)实验3中40分钟时反应达到平衡状态,所以υ(正) =υ(逆)。答案:=。
(6) 实验4中50分钟时反应达到平衡状态,由A的起始量1.0mol·L-1,平衡量0.15 mol·L-1,则A的变化量为0.85 mol·L-1;根据2A(g)![]() B(g)+D(g)知 B的变化量为0.425mol/L,由于B起始为0,则实验4中50分钟时B的浓度为0.425 mol/L。答案:0.425 mol/L。
B(g)+D(g)知 B的变化量为0.425mol/L,由于B起始为0,则实验4中50分钟时B的浓度为0.425 mol/L。答案:0.425 mol/L。