题目内容
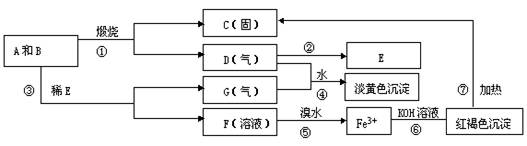
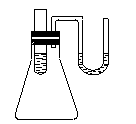
如右图所示,小试管内盛有约3 mL饱和硫酸铜溶液,与锥形瓶连通的U形管内盛有少量水(为便于观察,预先染成红色),沿小试管的内壁小心地慢慢倒入约3 mL 浓硫酸,静置片刻。以下描述不正确的是()

| A.小试管内液体分成两层,上层蓝色,下层无色 |
| B.U形细管内左边液面下降,右边液面升高 |
| C.有少量的白色固体析出 |
| D.以上现象都没有,无明显变化 |
D
浓硫酸的密度比饱和硫酸铜溶液的密度大,沿小试管的内壁小心地慢慢倒入的浓硫酸会沉在底部;浓硫酸溶于水放出大量热,使锥形瓶内密闭的气体受热膨胀,从而导致U形细管内左边液面下降,右边液面升高;浓硫酸具有吸水性和脱水性,水的减少导致有白色的无水CuSO4析出。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 KOH+I2+O2(未配平),下列说法正确的是( )
KOH+I2+O2(未配平),下列说法正确的是( )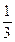 mol的氧原子化合价发生了变化
mol的氧原子化合价发生了变化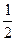 O2(g)
O2(g) SO3;ΔH="-98.3" kJ·mol-1放出的热量能在生产过程中得到充分利用,则每生产1 t 98%的硫酸只需外界提供(或可向外界输出)多少千焦热量?(H2SO4的摩尔质量为98 g·mol-1)
SO3;ΔH="-98.3" kJ·mol-1放出的热量能在生产过程中得到充分利用,则每生产1 t 98%的硫酸只需外界提供(或可向外界输出)多少千焦热量?(H2SO4的摩尔质量为98 g·mol-1)