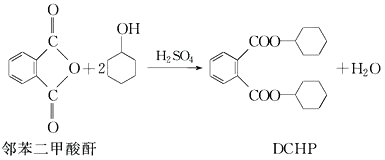
题目内容
【题目】下列化合物分子中,在核磁共振氢谱图中能给出一种信号的是( )
A.CH3CH2CH3
B.CH3COCH2CH3
C.CH3CH2OH
D.CH3OCH3
【答案】D
【解析】解:核磁共振氢谱中给出一种信号,说明该分子中有1种H原子;
A.CH3CH2CH3中有2种氢原子,核磁共振氢谱中有2种信号,故A错误;
B、CH3COCH2CH3中有3种氢原子,核磁共振氢谱中有3种信号,故B错误;
C、CH3CH2OH中有3种氢原子,核磁共振氢谱中有3种信号,故C错误;
D、CH3OCH3中有1种氢原子,核磁共振氢谱中有4种信号,故D正确;
故选D.

【题目】已知数据:
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 |
乙醇 | -117.3 | 78.5 | 0.789 |
乙酸 | 16.6 | 117.9 | 1.05 |
乙酸乙酯 | -83.6 | 77.5 | 0.90 |
浓硫酸(98%) | — | 338.0 | 1.84 |
实验室制取乙酸乙酯的主要步骤如下:①在30 mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸的混合溶液;②按图1连接好装置(装置气密性良好),用小火均匀地加热装有混合液的大试管3~5 min;③待试管B收集到一定量产物后停止加热,撤去试管B并用力振荡,然后静置分层;

图1
④分离出乙酸乙酯层、洗涤和干燥。
请根据题目要求回答下列问题:
(1)写出制取乙酸乙酯的化学方程式:________________________________________________________________________。
(2)上述实验中饱和碳酸钠溶液的作用是______(填字母代号)。
A.反应掉乙酸和乙醇
B.反应掉乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)步骤②中需要用小火均匀加热,其主要原因是________________________________________________________________________。
(4)某化学课外小组设计了图2所示的制取乙酸乙酯的装置(铁架台、铁夹、加热装置均已略去),
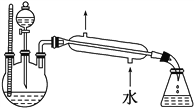
图2
与图1所示装置相比,此装置的主要优点有________________________________________________________________。
【题目】NiSO46H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Fe、Cr等杂质)为原料获得.工艺流程如图:
已知:25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表所示.
Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
Ksp | 8.0×10-16 | 4.0×10-38 | 6.0×10-31 | 6.5×10-18 |
完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |
请回答下列问题:
(1)下列措施可行,且能提高废渣浸出率的有___________。
A.升高反应温度
B.增大压强
C.在反应过程中不断搅拌
(2)在滤液Ⅰ中加入6%的H2O2 , 其作用是(用离子方程式表示);加入NaOH调节pH的范围是 , 为了除去溶液中的离子.
(3)滤液Ⅱ的主要成分是 .
(4)操作Ⅰ的实验步骤依次为:
①;
②向沉淀中滴加稀H2SO4 , 直至恰好完全溶解 ;
③蒸发浓缩、冷却结晶,过滤得NiSO46H2O晶体;
④用少量乙醇洗涤NiSO46H2O晶体并晾干。