题目内容
50 g镁、锌、铝的混合物与适量的稀硫酸反应,得三种盐的混合溶液,然后加热、蒸发、结晶得晶体(不含结晶水)218 g,则反应中得H2的质量为( )
| A.2 g | B.3 g |
| C.3.5 g | D.4.5 g |
C
无论是什么金属与稀硫酸反应,由硫酸的化学式可知,生成物中的n(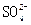 )=n(H2),所以金属与酸反应所得的无水晶体的质量就是金属与硫酸根离子的质量,
)=n(H2),所以金属与酸反应所得的无水晶体的质量就是金属与硫酸根离子的质量,
m(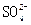 )="218" g-50 g="168" g,则氢气的质量为:
)="218" g-50 g="168" g,则氢气的质量为:
m(H2)=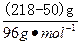 ×2 g·mol-1="3.5" g。
×2 g·mol-1="3.5" g。
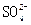 )=n(H2),所以金属与酸反应所得的无水晶体的质量就是金属与硫酸根离子的质量,
)=n(H2),所以金属与酸反应所得的无水晶体的质量就是金属与硫酸根离子的质量,m(
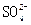 )="218" g-50 g="168" g,则氢气的质量为:
)="218" g-50 g="168" g,则氢气的质量为:m(H2)=
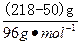 ×2 g·mol-1="3.5" g。
×2 g·mol-1="3.5" g。
练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
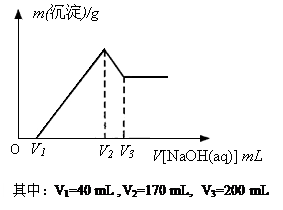
 ,向含a mol KAl(SO4)2的溶液中,逐滴加入Ba(OH)2溶液,过程中可能存在以下多个离子方程式
,向含a mol KAl(SO4)2的溶液中,逐滴加入Ba(OH)2溶液,过程中可能存在以下多个离子方程式
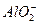 +2H2O
+2H2O