��Ŀ����
����Ŀ������ʵ�鷽�������л���۲���ȷ����
A. ��ʪ���pH��ֽ�ⶨ����Na2CO3��Һ��pH
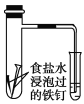
B. ͨ���۲���ͼ�е���ˮ���ı仯����֤�����������Ҫԭ����������ʴ
C. ��Mg(OH)2����Һ�еμ�FeCl3��Һ�����ֺ��ɫ������˵���ܽ�ȣ�Fe(OH)3��Mg(OH)2
D. ��ͬpH��ͬ����Ĵ����������Һ�м�������þ�ۣ�ͨ����ȫ��Ӧ���ռ�����H2������Ƚ�������ĵ���̶ȣ��������
���𰸡�A
��������
����A��Na2CO3��ǿ�������Σ���ˮ��Һ�У�CO32-����ˮ�ⷴӦ����ˮ���������H+���ٽ���ˮ�ĵ��룬�����մﵽƽ��ʱ����Һ��c(OH-)>c(H+),��Һ�Լ��ԣ���������ʪ���pH��ֽ�ⶨ����Na2CO3��Һ��pH������Һ��ϡ�����ã����� B���ھ�֧�Թ��з���һö��ʳ��ˮ���ݵ��������������к�������̼Ԫ�أ����Ծ�����ԭ��أ�����������������ʴ�������������������Թ��������ѹǿ��С���ұ�С�Թ��е�ˮ�ڴ���ѹǿ�������»����ŵ����������ƶ�һ�ξ��룬�γ�һ��ˮ�飬��˿�ͨ���۲�ͼ�е���ˮ���ı仯����֤�����������Ҫԭ����������ʴ����ȷ��C��Mg(OH)2��ˮ�����ܣ�Ҳ����һ�����ܽ�ȣ�����Mg(OH)2����Һ�еμ�FeCl3��Һ�����ֺ��ɫ������˵��Qc=c(Fe3+)��c3(OH-)>Ksp(Fe(OH)3)���ʿ���˵���ܽ�ȣ�Fe(OH)3<Mg(OH)2�����ܵ�������ܵ�ת������ȷ��D��ͬpH��ͬ����Ĵ����������Һ�е������ӵ����ʵ�����ȣ�����������þ�ۣ����߶�������Ӧ�������������������̶�С������Һ���յ�������������ӵ����ʵ�����Խ�ࡣ��Ӧ�����������������Խ������ͨ����ȫ��Ӧ���ռ�����H2������Ƚ�������ĵ���̶ȣ�����<���ᣬ��ȷ��

 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д�����Ŀ���¶�ΪTʱ����2.0 L�����ܱ������г���1.0 mol PCl5��������ӦPCl5(g)![]() PCl3(g)+Cl2(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ����
PCl3(g)+Cl2(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ����
t / s | 0 | 50 | 150 | 250 | 350 |
n(PCl3) / mol | 0 | 0. 16 | 0. 19 | 0. 20 | 0. 20 |
A. ��Ӧ��ǰ50 s ��ƽ��������(Cl2)= 0. 0032 mol��L-1��s-1
B. ���������������䣬�����¶ȣ�ƽ��ʱc(PCl3)= 0. 13 mol��L-1����Ӧ����H<0
C. ��ͬ�¶��£���ʼʱ�������г���1. 0 mol PCl5��0. 20 mol PCl3 ��0. 20 mol Cl2 ����Ӧ�ﵽƽ��ǰ��(��)<��(��)
D. ��ͬ�¶��£���ʼʱ�������г���2. 0 mol PCl3 ��2. 0 mol Cl2 ���ﵽƽ��ʱ��PCl3 ��ת���ʴ���80%


