题目内容
19.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )| A. | 常温下,23g NO2和N2O4的混合气体含有NA个氧原子 | |
| B. | 1L0.1mol•L-1的氨水含有0.1NA个OH- | |
| C. | 标准状况下,NO和O2各11.2L混合,所得混合气体的分子总数为0.75NA | |
| D. | 1molFe与1molCl2充分反应,转移3NA个电子 |
分析 A、NO2和N2O4的最简式均为NO2;
B、NH3•H2O为弱碱,在溶液中不能完全电离;
C、一氧化氮和氧气反应生成二氧化氮,二氧化氮能转化为四氧化二氮.
D、1molFe与1molCl2充分反应时铁过量,根据氯气的化合价的变化来分析转移电子的个数.
解答 解:A、NO2和N2O4的最简式均为NO2,故23g混合物中含有的NO2的物质的量为n=$\frac{23g}{46g/mol}$=0.5mol,则含有1mol氧原子即NA个,故A正确;
B、NH3•H2O为弱碱,在溶液中不能完全电离,故溶液中的氢氧根的个数小于0.1NA个,故B错误;
C、标况下,一氧化氮和氧气反应生成二氧化氮,二氧化氮能自身转化为四氧化二氮导致混合气体的分子总数小于0.75NA,故C错误;
D、1molFe与1molCl2充分反应时,铁过量,1mol氯气完全反应,由于氯元素由0价变为-1价,故1mol氯气转移2mol电子即2NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
15.亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危 害.其在酸性条件下会产生NO和NO2.下列有关说法错误的是( )
| A. | NaNO2既具有氧化性又具有还原性 | |
| B. | 1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol | |
| C. | NaNO2和胃酸作用的离子方程式为:2NO${\;}_{2}^{-}$+2H+=NO↑+NO2↑+H2O | |
| D. | 食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害 |
7.下表是元素周期表的一部分,针对表中的 种元素回答下列有关问题:
(1)在这些元素中,最活泼金属元素的原子结构示意图为 ,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).
,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).
(2)②、③、⑤、⑥、⑦形成的气态氢化物中最稳定的是HF(填化学式).
(3)④与②组成的某种化合物和①与②组成的某种化合物反应生成氧气,写出这两种化合物的电子式 ,
,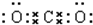 .
.
(4)用电子式表示元素④与⑥构成化合物的形成过程: 该化合物属于离子(填“共价”或“离子”)化合物.
该化合物属于离子(填“共价”或“离子”)化合物.
(5)能说明④与⑧金属性强弱的事实是分别与冷水反应,K与水的反应现象更剧烈,则钠比钾金属性的弱(举一例)
(6)设计实验方案比较⑥与⑦非金属性强弱
Cl2、S分别与H2反应
硫化钠和氯气反应.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 四 | ⑧ |
 ,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).
,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).(2)②、③、⑤、⑥、⑦形成的气态氢化物中最稳定的是HF(填化学式).
(3)④与②组成的某种化合物和①与②组成的某种化合物反应生成氧气,写出这两种化合物的电子式
 ,
,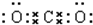 .
.(4)用电子式表示元素④与⑥构成化合物的形成过程:
 该化合物属于离子(填“共价”或“离子”)化合物.
该化合物属于离子(填“共价”或“离子”)化合物.(5)能说明④与⑧金属性强弱的事实是分别与冷水反应,K与水的反应现象更剧烈,则钠比钾金属性的弱(举一例)
(6)设计实验方案比较⑥与⑦非金属性强弱
Cl2、S分别与H2反应
硫化钠和氯气反应.
8.下列条件下,两瓶气体所含原子数一相等的是( )
| A. | 同质量的N2和CO2 | B. | 同质量的H2和N2 | ||
| C. | 同体积的O2和N2 | D. | 相同物质的量的N2O和CO2 |
9.下列有关实验的叙述正确的是( )
| A. | 用水润湿的pH试纸来测量溶液的pH | |
| B. | 实验需要480mL 2.0mol•L-1的氢氧化钠溶液.配制该溶液时先称量氢氧化钠固体38.4g,然后再按照溶解、冷却、移液、洗涤、定容、摇匀的步骤进行操作 | |
| C. | 向溶液中滴加硝酸酸化的Ba(NO3)2溶液出现白色沉淀,说明溶液中一定有SO42- | |
| D. | 用溴水,淀粉、KI溶液比较Br2与I2的氧化性强弱,所需玻璃仪器主要有:试管、胶头滴管 |
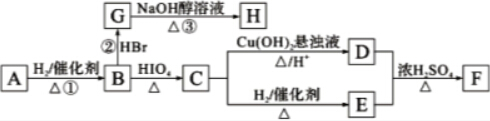
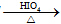 RCHO+R′CHO
RCHO+R′CHO .
. CH3COO-+NH4++2Ag↓+3NH3+H2O.
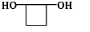
CH3COO-+NH4++2Ag↓+3NH3+H2O. .若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为
.若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为 .
. .
.
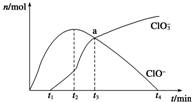 工业上把Cl2通入NaOH溶液中制得漂白液(主要成分NaClO).一化学小组模拟实验得到ClO-、ClO${\;}_{3}^{-}$等离子其物质的量(mol)与反应时间t(min)的关系曲线:
工业上把Cl2通入NaOH溶液中制得漂白液(主要成分NaClO).一化学小组模拟实验得到ClO-、ClO${\;}_{3}^{-}$等离子其物质的量(mol)与反应时间t(min)的关系曲线: