题目内容
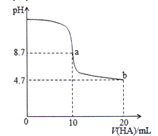
【题目】室温下,用滴定管量取一定体积的浓氯水置于锥形瓶中,用![]() 溶液以恒定速度来滴定,根据测定结果绘制出
溶液以恒定速度来滴定,根据测定结果绘制出![]() 、
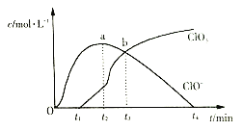
、![]() 等离子的物质的量浓度c与时间t的关系曲线如下。下列说法正确的是( )
等离子的物质的量浓度c与时间t的关系曲线如下。下列说法正确的是( )
A.![]() 溶液和浓氯水可以使用同种滴定管盛装
溶液和浓氯水可以使用同种滴定管盛装
B.a点溶液中存在如下关系:![]()
C.b点溶液中各离子浓度:![]()
D.![]() ,
,![]() 生成速率越来越快
生成速率越来越快
【答案】B
【解析】
A.![]() 溶液装在碱式滴定管中,由于浓氯水具有强氧化性,会腐蚀碱式滴定管下端的橡胶管,故浓氯水需用酸式滴定管来装,故A不正确;
溶液装在碱式滴定管中,由于浓氯水具有强氧化性,会腐蚀碱式滴定管下端的橡胶管,故浓氯水需用酸式滴定管来装,故A不正确;
B. a点溶液中存在电荷守恒式为:![]() ①,氯气与NaOH溶液发生氧化还原反应过程中的电子守恒:
①,氯气与NaOH溶液发生氧化还原反应过程中的电子守恒:![]() ,在同一溶液中,故有
,在同一溶液中,故有![]() ②,把②带入①中,可得如下关系:
②,把②带入①中,可得如下关系:![]() ,故B正确;
,故B正确;
C.b点溶液中根据B的分析可知,![]() ,发生的反应有Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O,结合图像,b点溶液中各离子浓度的大小关系应该为:
,发生的反应有Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O,结合图像,b点溶液中各离子浓度的大小关系应该为:![]() ,故C不正确;
,故C不正确;
D.在这个图中,反应速率是看曲线的斜率,故可以看出![]() ,后阶段
,后阶段![]() 生成速率是越来越慢,故D不正确;
生成速率是越来越慢,故D不正确;
故答案为:B。

【题目】短周期元素A、B、D、E、G、J在周期表中的位置如下:
A | |||||||
B | D | ||||||
E | G | J |
根据上表回答问题:
(1)![]() 在周期表中的位置是______,D的原子结构示意图_____。
在周期表中的位置是______,D的原子结构示意图_____。
(2)![]() 、B、E、G的原子半径由大到小的顺序是_____
、B、E、G的原子半径由大到小的顺序是_____![]() 填元素符号
填元素符号![]() 。
。
(3)![]() 、D的气态氢化物的稳定性关系为______
、D的气态氢化物的稳定性关系为______![]() 填化学式
填化学式![]() ,它们都属于______
,它们都属于______![]() 离子化合物或共价化合物
离子化合物或共价化合物![]() 。
。
(4)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的化学方程式________________。
【题目】Ⅰ.呋喃甲酸是一种抗生素,在食品工业中作防腐剂,也作涂料添加剂医药、香料等中间体,可用呋喃甲醛制备,其实验原理和制备步骤如下:
2![]() +NaOH→
+NaOH→![]() +
+![]() H<0
H<0
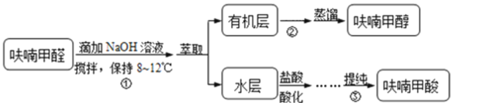
步骤③提纯过程:溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥。
(1)步骤①的关键是控制温度,其措施有:磁力搅拌、__________和缓慢滴加![]() 溶液。
溶液。
(2)步骤②中,加入无水![]() 的作用_______。
的作用_______。
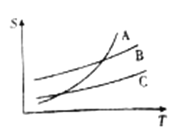
(3)呋喃甲酸在A、B、C三种溶剂中溶解度(S)随温度(T)变化的曲线如图。步骤③提纯时合适的溶解试剂是________。
Ⅱ.利用呋喃甲酸制取的呋喃甲酸正丁酯是一种优良的有机溶剂。某化学兴趣小组在实验室用呋喃甲酸和正丁醇制备呋喃甲酸正丁酯,有关物质的相关数据及实验装置如图所示:
化合物 | 相对分子质量 | 密度( | 沸点(℃) | 溶解度(g/100g水) |
呋喃甲酸 | 112 | 1.322 | 230-232 | 4.33 |
正丁醇 | 74 | 0.81 | 117.3 | 9 |
呋喃甲酸正丁酯 | 168 | 1.053 | 136.1 | 0.7 |
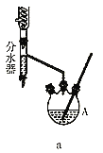

分水器的操作方法:先将分水器装满水(水位与支管口相平),再打开活塞,准确放出一定体积的水。在制备过程中,随着加热回流,蒸发后冷凝下来的有机液体和水在分水器中滞留分层,水并到下层(反应前加入的)水中;有机层从上面溢出,流回反应容器。当水层增至支管口时,停止反应。
呋喃甲酸正丁酯合成和提纯步骤为:
第一步:取足量的正丁醇和![]() 呋喃甲酸混合加热发生酯化反应,反应装置如图a所示(加热仪器已省略);
呋喃甲酸混合加热发生酯化反应,反应装置如图a所示(加热仪器已省略);
第二步:依次用水、饱和![]() 溶液、水对烧瓶中的产品洗涤并干燥;
溶液、水对烧瓶中的产品洗涤并干燥;
第三步:用装置b蒸馏提纯。
回答有关问题:
(4)装置A的名称_________。
(5)实验中使用分水器的优点有________。
(6)第二步用饱和![]() 溶液洗涤的目的是______。
溶液洗涤的目的是______。
(7)若实验中得到呋喃甲酸正丁酯![]() ,则呋喃甲酸正丁酯的产率为________。实验中呋喃甲酸正丁酯的实际产率总是小于此计算值,不可能原因是_______(填字母代号)。
,则呋喃甲酸正丁酯的产率为________。实验中呋喃甲酸正丁酯的实际产率总是小于此计算值,不可能原因是_______(填字母代号)。
A.分水器收集的水里含呋喃甲酸正丁酯
B.该实验条件下发生副反应
C.产品精制时收集部分低沸点物质
D.产品在洗涤、蒸发过程中有损失