题目内容
【题目】KMnO4是一种用途广泛的氧化剂,可由软锰矿(主要成分为MnO2)通过下列方法制备:
①软锰矿与过量KOH、KC1O3固体熔融生成K2MnO4;②溶解、过滤后将滤液酸化,使K2MnO4完全转变为MnO2和KMnO4;③滤去MnO2,将滤液进行处理可获得深紫色的KMnO4产品。
(1)制备过程中,为了提高原料的利用率,可采取的措施是___________________。
(2)写出第②步中发生反应的离子方程式____________。
(3)第③步中从滤液中获得KMnO4晶体的方法是______、_______、过滤、洗涤、干燥。
(4)取上述制得的KMnO4产品2.0000g,溶于水配成250mL溶液,取出25.00mL于碘量瓶中,加入稀硫酸和足量碘化钾并放于暗处5min左右,然后加入适量水和数滴淀粉溶液作指示剂,用0.2500mol/L标准Na2S2O3溶液进行滴定(发生反应I2+2S2O32-=2I-+S4O62-,杂质不参加反应),滴定至终点消耗Na2S2O3溶液20.00mL。
①滴定终点的现象是_____________。
②计算KMnO4产品的纯度。(写出计算过程)_____________
【答案】将③中MnO2回收利用3MnO42-+4H+=MnO2↓+2MnO4-+2H2O蒸发浓缩降温结晶当加入最后一滴标准Na2S2O3溶液时,溶液由蓝色变为无色,且半分钟内不变色79%
【解析】
(1)将步骤③中MnO2回收,再发生步骤①中的反应,可以提高MnO2利用率;
(2)根据反应物与生成物来书写反应方程式;
(3) 第③步中从滤液中获得KMnO4晶体的方法是蒸发浓缩、降温结晶、过滤、洗涤、干燥;
(4)根据滴定原理分析终点现象,利用反应方程式及Na2S2O3的量来计算KMnO4产品的纯度。
(1)将步骤③中MnO2回收,再发生步骤①中的反应,可以提高MnO2利用率;
因此,本题正确答案是:将③中MnO2回收利用;
(2)由滤液酸化后,K2MnO4完全转变为MnO2和KMnO4,则反应的离子方程式为3MnO42-+4H+=MnO2↓+2MnO4-+2H2O,
因此,本题正确答案是:3MnO42-+4H+=MnO2↓+2MnO4-+2H2O;
(3) 第③步中从滤液中获得KMnO4晶体的方法是蒸发浓缩、降温结晶、过滤、洗涤、干燥,因此,本题正确答案是:蒸发浓缩;降温结晶;
(4) ①碘与淀粉显蓝色,则滴定终点的现象是当加入最后一滴标准Na2S2O3溶液时,溶液由蓝色变为无色,且半分钟内不变色,
②消耗硫代硫酸钠的物质的量n=cV=0.025L![]() 0.02L=0.005mol,根据得失电子守恒知高锰酸钾的物质的量=0.005mol
0.02L=0.005mol,根据得失电子守恒知高锰酸钾的物质的量=0.005mol![]() 5=0.001mol,
5=0.001mol,
所以m(KMnO4)=nM=0.001mol×158g/mol=0.158g,
KMnO4产品的纯度为:![]() ×100%=79%;
×100%=79%;
因此,本题正确答案是:当加入最后一滴标准Na2S2O3溶液时,溶液由蓝色变为无色,且半分钟内不变色;79%。

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案【题目】下列有关实验操作、现象和解释或结论有错误的是( )
选项 | 实验操作 | 现象 | 解释或结论 |
A | 少量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
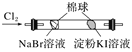
B |
| 左边棉球变为橙色,右边棉球变为蓝色 | 证明氧化性:Cl2>Br2,但不能证明氧化性:Br2>I2 |
C | 向某溶液中加入硝酸银溶液 | 产生白色沉淀 | 则溶液有氯离子 |
D | 浓HNO3加热 | 有红棕色气体产生 | HNO3有不稳定性 |
A. AB. BC. CD. D