��Ŀ����
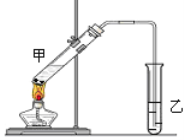
����Ŀ��Ϊȷ��ij���ȼ���������������������ɣ��ֱ��������ʵ�顣
��1����ȡa g��Ʒ�������м���������NaOH��Һ��������ɵ����壨��״������ͬ�����Ϊb L����Ӧ�����ӷ���ʽΪ ��
��2����ȡͬ����a g��Ʒ���ڸ�����ǡ����ȫ��Ӧ��
��3������2���з�Ӧ������ȴ�����������ᣬ������ɵ��������Ϊc L���������루1�����������������ȣ�c��bΪ_______________��
��������ʵ���ȷ�������ȼ��к�Al����������Ϊ ��
���𰸡���1��2Al +2OH-+2H2O =2AlO2-+3H2�� ��3��2 : 3 25.23%����27/107��
�������������������1��������Ӧ��2Al+2NaOH+2H2O�T2NaAlO2+3H2�������ӷ���ʽΪ��2Al+2OH-+2H2O�T2AlO2-+3H2��������bL���������ʵ���Ϊ![]() =
=![]() mol���ɷ���ʽ��֪Al�����ʵ���Ϊ
mol���ɷ���ʽ��֪Al�����ʵ���Ϊ![]() mol������Al������Ϊ
mol������Al������Ϊ![]() mol����27g/mol=
mol����27g/mol=![]() g��
g��
��3���ɷ���ʽ��֪��Al��Fe�����ʵ�����ȣ����ݵ���ת���غ㣬��֪�루1���������������֮��Ϊ2��3�����ݷ�Ӧ2Al+Fe2O3![]() 2Fe+Al2O3����֪������������������Ϊ160��54=80��27��������ȼ���Al����������Ϊ
2Fe+Al2O3����֪������������������Ϊ160��54=80��27��������ȼ���Al����������Ϊ![]() ��100%=25.23%��
��100%=25.23%��

 ������ȫ�̼����ĩ���100��ϵ�д�
������ȫ�̼����ĩ���100��ϵ�д�