题目内容
(2013?泰安一模)下列说法中,正确的是( )
分析:A.无氧酸的酸性强弱与得电子能力没有必然联系;
B.第二周期中O、F没有正价;
C.同周期元素原子的最外层电子数越多,非金属性越强;
D.含离子键的化合物一定为离子化合物,共价化合物中只能存在共价键.
B.第二周期中O、F没有正价;
C.同周期元素原子的最外层电子数越多,非金属性越强;
D.含离子键的化合物一定为离子化合物,共价化合物中只能存在共价键.
解答:解:A.无氧酸的酸性强弱与得电子能力没有必然联系,酸性及得电子能力比较均正确,但没有因果关系,故A错误;
B.第二周期中O、F没有正价,O、F除外,第二周期元素的最高正化合价从左到右依次升高,故B错误;
C.同周期元素原子的最外层电子数越多,非金属性越强,其氢化物稳定性越强,选项中没有指明同周期,则最外层电子数多,其非金属性不一定强,故C错误;
D.含离子键的化合物一定为离子化合物,共价化合物中只能存在共价键,不能含离子键,故D正确;
故选D.
B.第二周期中O、F没有正价,O、F除外,第二周期元素的最高正化合价从左到右依次升高,故B错误;
C.同周期元素原子的最外层电子数越多,非金属性越强,其氢化物稳定性越强,选项中没有指明同周期,则最外层电子数多,其非金属性不一定强,故C错误;
D.含离子键的化合物一定为离子化合物,共价化合物中只能存在共价键,不能含离子键,故D正确;
故选D.
点评:本题考查非金属元素在周期表中的性质变化规律,注意把握周期表中一般规律及特例来分析解答,选项C为解答的易错点,题目难度中等.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案
相关题目
 (2013?泰安一模)用选项中的电极、溶液和如图所示装置可组成原电池.下列现象或结论叙述正确的是( )
(2013?泰安一模)用选项中的电极、溶液和如图所示装置可组成原电池.下列现象或结论叙述正确的是( )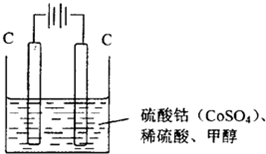 (2013?泰安一模)研究碳及其化合物的性质对促进低碳社会的构建具有重要意义.
(2013?泰安一模)研究碳及其化合物的性质对促进低碳社会的构建具有重要意义.