��Ŀ����
��ҵ�Ϻϳɰ���ԭ��֮һ������������һ����Դ��ȡ��ʯ�������������������������������ش��������⣺
��1��������������·�Ӧ;�������跴Ӧ���ܽ��У�����Ϊ��������ǣ� ��
A.
B.
C.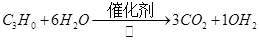
D.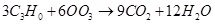 ��
��
��2��������������ķ�Ӧ;������������1mol������Ƶð��� ����
A��4mol B��6.7mol C��10 mol D��2.7mol
��3���ú����ķ�Ӧ;�����������ŵ��ǣ� ����
A�������� B���Ƶõ�H2���ȸ�
C����ȡH2�IJ����� D����ͬʱ��ô�������
��1��C ��2��B ��3��C
��������
�����������1��A��B��D����������Ҫ��������Ҫ�ṩ����������ߣ������ϲ����㡣
��2������������ķ�����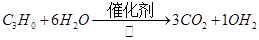 ���ϳɰ��ķ�ӦΪ��
���ϳɰ��ķ�ӦΪ��
3H2+N2 2NH3���ɴ���������ʽ�ɵó���ϵʽ��C3H8��10H2��
2NH3���ɴ���������ʽ�ɵó���ϵʽ��C3H8��10H2��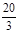 NH3����ˣ�1mol������Ƶð���Լ6.7mol��
NH3����ˣ�1mol������Ƶð���Լ6.7mol��
���㣺������Ҫ�������û�ѧ����ʽ�ļ��㡣
�����������ǶԻ�ѧ����ʽ����Ŀ��顣������Ӧע�����µ�λӦһ�£�ͬʱ�����ڶಽ��Ӧ�ļ��㣬�����м�����ҳ���ʼ��Ӧ��������������֮��Ĺ�ϵʽ���Ӷ�������㣬���ټ�������


 CO��g��+3H2��g������H=+QkJ/mol��Q��0��
CO��g��+3H2��g������H=+QkJ/mol��Q��0�� ��ѧ����Դ��������������ʮ�ֹؼ������ã�������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϣ�
��ѧ����Դ��������������ʮ�ֹؼ������ã�������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϣ� ��ѧ����Դ����������������ʮ�ֹؼ������ã�������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϣ�
��ѧ����Դ����������������ʮ�ֹؼ������ã�������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϣ�
 2NH3 (g) ��H����92.2kJ��mol��1
2NH3 (g) ��H����92.2kJ��mol��1